Köpek ve Kedilerde Aşılama Gerçekleri
(1) Dünyadaki tüm aşılar, Cor aşılar (yapılması zorunlu) ve yapılması zorunlu olmayan aşılar diye ayrılmıştır. Cor aşılar içerisinde köpek karma aşısı ve kedi karma aşısı yer alır. Kuduz hastalığının olduğu yerlerde kuduz aşısı da Cor aşı olarak kabul edilmelidir. Kuduz riski varsa, karma ve kuduz yapılması zorunlu olan aşılardır.
(2) Normal şartlarda kuralına uygun bir aşılama köpek ve kedilerde minimum üç yıl hatta ömürlük bağışıklık sağlayabilir. Ticari olarak yapılan antikor bazlı testler hastalık taramak için değil aşının etkinliğini kanıtlamak için yapılmalıdır.
(3) Hayvanlarda temel olmayan; Corona, Bronchine, Lyme vb. aşılar risk halinde yapılmalıdır. Bu aşılar genelde 1 yıllık immunite sağlar, takip edilerek yıllık tekrarlanmalıdır.
(4) Bazen ülke ruhsatlandırılması aşının yılda bir yapılmasını önermektedir, bunun farklı nedenleri olmaktadır. Köpek ve kedinin sahibi bu önerinin sadece kendi onayıyla yapıldığını anlamalı ve sorumluluğu üstlenmelidir. Kuşku halinde yıllık antikor taramaları mantıklı bir yoldur.
(5) Bu klavuzun amacı köpek ve kedilerinizi gereksiz aşı yükünden kurtarmanız; hem onlar için sağlıklı hem sizin için ekonomik avantaj elde etmenizdir. Bütün hayvanları temel aşılarla aşılamalıyız, temel olmayanlardan ise gerekmedikçe kaçınmalıyız.
(6) Bir köpeğe yapılacak aşı köpek 4 aydan küçükse maternal antikor, immun yeterlilik vb. kurallara bağlı olarak yeterli direnç oluşturmaz. Aşılama programına hangi hasta başlarsa başlasın 4 ayı geçince karma aşı tekrarlanmalıdır.
(7) Temel aşılar dışında olan Lyme, Bronchine, Corona vb. aşıları daha sık uygulamayla direnç oluştururlar. Bu aşıların takibi halinde yılda bir uygulama gereklidir.
(8) Kuduz aşısı yasal zorunluluk gereği yılda bir yapılmalıdır bu aşı bazı ülkelerde 3 yılda bir yapılmaktadır. Kuduz aşısı, Cor aşı grubundadır.
(9) Speed testlerin ekonomik yükü daha fazla olduğu için test yaptırmak yerine köpek ya da kedilere aşı yapılmaktadır. Normalde testler negatifse aşı gerekli, pozitifse gereksizdir. Sağlıklarıyla ilgili gereksiz yapılan her aşı riski göze almaktır.
(10) Antikor testleri aşının çalıştığını gösteren tek testtir, birçok nedenle aşı çalışmayabilir.
(11) Parvoglob, Febriglob gibi immun plazma uygulamalarının, hastalık semptomları görüldükten sonra kullanılması anlamsızdır. Bunlar semptom göstermeyen risk altındaki hayvanlara yapılmalıdır.
(12) Kedileri, risk altında toplu yaşayan ve risksiz grup olarak ikiye ayırmalıyız. Karma aşısı 3-7 yıl arasında bağışıklık sağlasa da risk altındaki hayvanlara yılda bir yapılması önerilmektedir.
(13) FLV aşılamak için hayvanın negatif olduğundan emin olunmalıdır ve hayvan risk altındaysa yapılmalıdır.
(14) Adjuvan aşılar kedilerde sarkom tetikleyebilir, yapıldıkları yerler önemlidir.
(15) Gençlik dönemlerinde düzgün aşılanmış hayvanların yaşlılık dönemlerinde aşılamaya ihtiyaç duyulmaz.
(16) Köpekleri canlı aşılarla aşılamak en az 5 yıl bağışıklık sağlar.
(17) 4 aydan büyük bir köpekte karma aşı, 26. ve 52. haftada yapılırsa 3 yıl aşı gereksizdir.
Kedi ve Köpeklerde Aşı Uygulamalarıyla İlgili Kılavuz
(1)Bristol Üniversitesi, Birleşik Krallık
(2)(Eskiden) Utrecht Üniversitesi, Hollanda
(3)Wisconsin Üñiversitesi-Madison, Wisconsin, A.B.D.
(4)James Cook Universitesi , Queensland, Avustralya
iletişim: M. J. Day [email protected]
ÖZET
VGG (WSAVA Vaccination Guidelines Group) kedi ve köpeklere aşı yapılmasıyla ilgili küresel düzeyde bir kılavuz oluşturmak için bir araya gelmiştir. İlk versiyonu 2007 yılında basılmış, 2010 yılında güncellenmiştir. Elinizdeki bu kitapçık daha önceki versiyonların en güncel hali olup, yapılan yeni eklerle geliştirilmiştir, küçük hayvanların aşılanmasıyla ilgili uluslararası geçerliliği olan bir kılavuz oluşturmakta ve burada yapılan öneriler bilimsel kanıtlarla desteklenmektedir. Kurumumuz hayvan bakımının ülkeden ülkeye ekonomik şartlara bağlı olarak farklılıklar gösterebileceğini kabul etmektedir. Bu kılavuzda yer alan bilgiler zorunlu olmamakla birlikte, ulusal düzeyde dernekler veya veterinerler tarafından ülke şartlarına uygun şekilde uyarlanmalıdır. Kurumumuz mümkün olduğu takdirde tüm kedi ve köpeklerin aşılanmasını önermektedir. Bu sadece bireysel düzeyde hayvanı korumaz, aynı zamanda tüm hayvanların bulaşıcı hastalık salgınından korunmasını sağlar.
Tüm bunları göz önünde bulundurduğumuzda, VGG tüm kedi ve köpeklere, bulundukları coğrafi alan veya şartlardan bağımsız olarak mutlaka yapılması gereken aşıları temel aşı olarak tanımlamıştır. Bu aşılar hayvanları; yayılma tehlikesi olan, hayatlarını tehdit edici boyutta ciddi hastalıklara karşı korurlar. Bu aşılar, köpekler için canine distemper virus (CDV) ya da gençlik hastalığı, canine adenovirus (CAV) ve canine parvorius tip2 (CPV-2) nin değişik formlarıdır. Kediler için temel aşılar, feline parvovirus (FPV) ya da kedi gençlik hastalığı, feline calicivirus ( FCV) ve feline herpesvirus-1 (FHV-1) dir. Kuduz aşısı her ülkede yasal bir zorunluluk değildir, ancak kuduz virüsünün görüldüğü yerlerde, kedi ve köpekler mutlaka aşılanmalıdır. (1)
VGG anne tarafından geçen antikorların (maternally derived antibodies-MDA) yavru köpek ve kedilere yapılacak bu aşıların etkinliğini etkilediğini kabul etmiştir. Bu antikorların miktarı bir batında doğan yavrular arasında büyük farklılıklar gösterir. Bu nedenle VGG, bu aşıların yavrulara 16 haftaya kadar yapılmasını ve 6. Veya 12. aylarda tekrarlanmasını önermektedir. Ekonomik ve bölgesel şartların el vermediği durumlarda sadece bir doz temel aşı 16. haftalık veya daha büyük yavrulara uygulanabilir.
VGG, temel aşıdan sonra (CDV,CAV, CPV-2, ve FPV) bağışıklığın gelişip gelişmediğini görmek veya barınaklardaki salgın hastalıkları engellemek için basit bazı testler uygulanmasını desteklemektedir.
Aşılar gereksiz yere kullanılmamalıdır. Yukarıda belirttiğimiz temel aşılar, yavru köpek ve kedilere 6. veya 12. ayda tekrar yapıldıktan sonra, 3 yıldan önce tekrarlanmamalıdır. Çünkü bu aşıların bağışıklık süresi birkaç yıldır, hatta ömür boyu bile olabilir. (2)
VGG temel olmayan aşıları şu şekilde tanımlar: hayvanların bulunduğu yer ve yaşam tarzı, içinde bulunduğu riskler, bu hayvanları çeşitli enfeksiyon riskleriyle karşı karşıya bırakıyorsa bu durumda, temel olmayan aşılardan bahsedilir. VGG bazı aşıları da yeterli bilimsel temel olmadığı için önermemektedir.
VGG düzenli olarak(yıllık) yapılacak sağlık kontrolünü desteklemektedir. Bu senelik kontrollerde, temel olmayan aşılar yapılabilir. Zaten bu aşıların koruma süreleri genellikle 1 yıldır. (3)
VGG barınaklardaki aşı uygulama şartlarını da olabildiğince basite indirgemiştir: Barınağa giriş yapan tüm kedi ve köpekler barınağa girmeden önce veya giriş tarihleri itibariyle temel aşılarla aşılanmalıdır. Ekonomik olanaklar elverdiğinde, kılavuzda belirtildiği şekilde temel aşılar tekrarlanmalıdır. Solunum yolları hastalıklarına yönelik temel olmayan aşılar da yapılabilir.
Mümkün olduğu durumlarda veterinerler, görülen yan etkileri üretici firmalara veya yetkili kurumlara iletmelidir. Bu sayede, aşının güvenilirliği arttırılır.
Sonuç olarak, tüm kedi ve köpekler temel aşılarla aşılanmalıdır; temel olmayan aşılarsa gerekli görülmedikleri durumlarda yapılmamalıdır.
Köpek ve Kedilerde Aşılama Gerçekleri GİRİŞ
Bu grup, 2006 yılında, kedi ve köpekler için küresel bir aşılama kılavuzu oluşturmak için bir araya gelmiştir. Bunu oluştururken de bu hayvanların bakımlarıyla ilgili ekonomik ve sosyal farklılıkları göz önünde bulundurmuştur. Bu nedenle, bu kılavuz Kuzey Amerika’da hazırlanan kılavuzlardan ve Avrupa’daki Advisory Board of Feline Disease tarafından hazırlanan kılavuzlardan kapsam bakımından daha geniştir. İlk kılavuz 2007 yılında basılmış (Day ve diğerleri, 2007) ve 2010 yılında güncellenmiştir (Day ve diğerleri 2010). 2011-2013 arasında, VGG kedi ve köpekleri etkileyen enfeksiyona bağlı hastalıklara ve Asya kıtasındaki aşılamaya odaklanmış ve Asya kıtasındaki veterinerler için yerel düzeyde aşılamayla ilgili önerilerde bulunmuştur. 2014 ve 2015’ te uluslararası aşılama kılavuzunun yenilenmesi ve güncellenmesi alanında çalışmalarda bulunmuştur. Bu çalışmanın sonuçları elinizdeki kitapçığı oluşturmaktadır.
1. Kanıta dayalı öneriler oluşturmaya özellikle dikkat edilmiştir; bunun yanısıra, yeni bir sınıflandırma şeması oluşturulmuştur ve eskiye göre bilimsel literatüre yapılan atıflar detaylı hale getirilmiştir.
2. Anneden geçen antikorlar yavru kedi ve köpeklerde dikkate alınmıştır, bu yüzden yavruların aşı takvimlerinin başlangıç tarihinde değişikliğe gidilmiştir. Yavrulara yapılacak aşı serisinde son aşı tarihi 16 hafta veya sonrasına bırakılmıştır.
3.Yavru kedilere yapılan booster (tekrar) aşısının zamanlamasında değişiklik yapılmıştır. Bu değişiklikle, booster aşısının 26 haftalıkken yapılma opsiyonu getirilmiştir.
4. Yetişkin kedilerde FHV-1 e ve FCV’ye karsı yapılan canlı virüslü aşıların tekrarıyla ilgili bilgiler açıklığa kavuşturulmuş ve daha detaylı hale getirilmiştir.
5. Yeni aşılar hakkında bilgiler dahil edilmiştir (köpekler için oral yolla uygulanan bordetalla bronchiseptica aşısı, 2 tür virus bulunduran FCV aşıları ve farklı serogruplardan oluşan leptospira aşısı)
6. FIV aşısı temel olmayan aşılar kapsamına alınmıştır.
7. Barınaklarda yaşayan yavru kedi ve köpekler için temel aşı zamanları yeniden belirlenmiştir.
8. Evde uygulanabilen test kitleri ayrıntılı olarak ele alınmıştır.
9.VGG hastalık belirtileri sayfası güncellenmiştir ve sıkça sorulan sorular genişletilmiştir.
KANITA DAYALI VETERİNER HEKİMLİK
Kanıta dayalı veteriner hekimlik (KDVH) kavramı, WSAVA aşı kılavuzunu yayımladığı 2007 tarihinden itibaren öne çıkmaya başlamıştır. Herhangi bir prosedürü ortaya koyan kanıtların ağırlıklandırılması daha önce Avrupa’da kedilerin aşılanması üzerine çalışması bulunan Lloret(2009) tarafından yapılmıştır. VGG elinizdeki bu kitapçıkta daha açık bir kanıta bağlı yaklaşım sergilemektedir. Böylece uygulayıcı veterinerler öneriye temel oluşturan kanıtın farkına varırlar. Bu yüzden bu kitapçık öncekilere göre tam bir şekilde atıflandırılmıştır. Ek olarak, VGG destekleyici kanıtlar için bir sıralama oluşturmak istemiş, ancak mevcut şemaların aşılama alanına uygulanabilirliklerinin düşük olduğu görülmüştür. Bu yüzden VGG kendi KDVH sistemini oluşturmuştur.
Tip 1 kanıt[EB1]: Hakem denetimli bilimsel yayınlara atıfta bulunulduğu durum. Bu durumda ortaya konulan kanıt, hakem denetimi olmasına rağmen farklı nitelikte bilimsel kalitededir, çünkü hakem denetimi için genel geçer standartlar bulunmamaktadır.
Tip 2 kanıt[EB2]: Yayınlanmamış ticari araştırmalara bağlı kanıt. Bu araştırmalar veteriner aşıları için ruhsat almanın düzenleyici bir parçasıdır. Burda, prospektüste yer alan bilgiler düzenleyici otoritenin hakemleri tarafından gözden geçirilir.
Tip3 kanıt[EB3]: Hakemli bilimsel dergilerde yayımlanmamış, yasal prosedürün bir parçası olarak denetlenmemiş ticari ya da bağımsız deneyler tarafından desteklenen sonuçlar.
Tip 4 kanıt[EB4]: Deneysel veya alan çalışmalarınca desteklenmeyen ancak mikrobiyoloji, immunoloji veya genel kanı tarafından desteklenen düşünceler.
Bu kitapçıkta yapılan önermeleri [EB1], [EB2],[EB3],[EB4] şeklinde kısaltmalar takip edecektir. Bu atıfta bulunulan kaynağın kategorisini gösterir. Her durumda mevcut olan en yüksek kategori belirtilecektir.
Köpek ve Kedilerde Aşılama Gerçekleri KILAVUZUN AMACI
Bu kitapçık kedi ve köpeklere yapılan aşılarla ilgili genel geçer kurallar ileri sürmemektedir. Çünkü WSAVA’ya üye 80 ülkenin arasında enfeksiyona bağlı hastalıkların mevcudiyeti, aşıların sağlanabilirliği, sahipli sahipsiz hayvan oranı, uygulamalar ve ekonomik ve sosyal şartlar bakımından farklılıklar bulunmaktadır.
Bu kitapçık ulusal çaptaki küçük hayvan veterinerlik birliklerine ve WSAVA üyelerine güncel bilimsel öneri sağlamayı ve örnek aşı uygulamaları göstermeyi amaçlamaktadır. Bu kitapçığı okumak, üzerinde tartışıp uygulamak veterinerlerin kişisel isteklerine bırakılmıştır.
Uygulayıcı hekimler bazen bu kılavuzdaki bilgilerle ürün bilgi sayfalarının çeliştiğini görürler ve eğer kılavuz önerilerini uygularlarsa sorun çıkacağını düşünürler. Thiry ve Horzinek (2007) tarafından prospektüs ve kılavuz arasındaki farklar belirtilmiştir.
Prospektüs veya SPC (summary of product characteristics) bir aşının kayıt altına alınması prosedürüne aittir. Prospektüs bir ürünün kalitesi, güvenilirliği veya etkinliği hakkında bilgi verir, aşılar söz konusu olduğundaysa aşıların en az koruma sürelerini belirtir. Aşıların koruma süreleri deneysel kanıtlara bağlıdır ( örneğin bir aşı yapıldıktan sonra, hayvan enfeksiyon veya hastalıktan ne kadar süre korunuyor?). Evcil hayvanlara yapılan çoğu aşının, yakın zamana kadar 1 yıllık koruma süresi olduğu söylenmiş ve her yıl tekrarlanması önerilmiştir. Son yıllarda, aynı aşıların büyük bir çoğunluğu en az 3 yıllık koruma süresiyle ruhsatlanmıştır ( bazen de 4 yıl). Aslında çoğu ülkede MLV (modified Live Virus) aşılarının büyük çoğunluğu yetişkin hayvanlar söz konusu olduğunda 3 yılda bir aşı tekrarı koşuluyla ruhsatlanmıştır. Öte yandan, bazı ülkelerde aynı ilaçlar 1 yıllık koruma süresine sahiptir. Bunun sebebi basittir. Üretici firma ürününün öneriler bölümünü (label recommendation) değiştirmemiştir ya da o ülkede ruhsat veren otorite değişikliğin yapılmasına izin vermemiştir. Bu durum o ülkedeki uygulayıcı veterinerler arasında karışıklık yaratır. Unutulmamalıdır ki 3 yıllık koruma süresi bile temel aşılar için minimum koruma süresidir, bu aşıların büyük çoğunluğunda koruma süresi ömür boyu olmasa da, 3 yıldan çok daha uzundur.
Bu nedenle, bu kitapçığın 3 yıl veya daha az sıklıkta yinelenmesini önereceği ancak aşının ruhsatının 1 yıllık koruma süresi olduğu durumlar olacaktır. Bu durumlarda, veterinerler aşıları bu kitapçığın önerilerine göre yapmalı, öte yandan hayvan sahibini bilgilendirip yazılı onayını almalıdır. Veterinerler ayrıca, ilaç firması mümessillerinini ruhsatlarına uygun olarak kendi prospektüs ve ruhsatlarındaki süreyi önereceklerini unutmamalıdır.
Veterinerler farklı ülkelerdeki yerel uzmanların, grupların özellikli enfeksiyonel hastalıklar hakkındaki fikirlerini de dikkate aldığı durumlarda karışıklık artabilir. VGG de çok sayıdaki yerel ve ulusal kılavuz arasından bir orta yol bulmakta zorlanmaktadır. Bu kılavuzdaki öneriler kedi ve köpekler için küresel çaptaki farklılıkları en aza indirmeyi ve dengeli bir bakış açısı sağlamayı amaçlamaktadır.
Sonuç olarak veterinerler, bu kılavuzda verilen aşılama aralıkları ve sürelerine uygun olarak aşı yapabilirler. Ancak yerel önerilerle de karşılaştırma yapmalıdırlar. VGG önerileri ilaç üzerindeki önerilen süreden farklıysa, VGG önerilerini uygulamadan önce, veteriner müşterisini bilgilendirmeli ve yazılı onayını almalıdır. (4)
Küçük hayvanların aşılanmasındaki mevcut sorunlar
Eğer aşılar bu kadar başarılıysa, neden aşı uygulama prosedürü sürekli gözden geçiriliyor ve yenileniyor? Gelişmiş ülkelerde, kedi ve köpekleri etkileyen enfeksiyona bağlı hastalıkların nadir olduğu bir gerçektir. Ancak bu ülkelerde bile, bu enfeksiyonların daha sık görüldüğü bölgeler veya ara sıra rastlanan salgın hastalıklar olmaktadır. Ayrıca sahipsiz hayvanlar veya barınaklardaki hayvanların durumlarını sahipli hayvanlardan farklı olarak ele almak gerekir. Gelişmekte olan ülkelerde küçük hayvanlarda enfeksiyona bağlı hastalıklar sık görülür ve bu hastalıklar hayvanlardaki en büyük ölüm sebeplerinden biridir. Sağlıklı rakamlar elde etmek zor olsa da, gelişmiş ülkelerde evcil hayvanların aşılanma oranı % 30- 50 arasındadır. Gelişmekte olan ülkelerdeyse bu oran çok daha düşüktür. 2008 Global Ekonomik Krizini izleyen dönemde, bunun bir etkisi olarak aşı uygulamalarında da azalma görülmüştür (2013).
Küçük hayvan veterinerlik bilim dalında, topluluk bağışıklığı kavramını ele almakta geç kaldık; bu kavramda her hayvanın aşılanması önemlidir, çünkü sadece hayvan korunmaz, o çevredeki popülasyonda hastalığa sebep olabilecek hayvan sayısı ve hastalığın yayılma riski azalmaktadır. Birkaç yıl koruma sağlayan aşılarla hayvan topluluğu bağışıklığı oluşturmak, o topluluktaki hayvanların aşılanma oranına bağlıdır, her yıl ne kadar aşı kullanıldığına bağlı değildir. Bu nedenle kedi ve köpekler aşılanırken, toplam aşılı hayvan oranı arttırılması hedeflenmelidir. Bir hayvanın bireysel olarak bağışıklığı yinelenen aşılarla mümkün değildir. 3 senede bir MLV aşısı yapılan bir köpek her sene yapılan bir köpekle eşit derecede bağışıklıga sahiptir (Bohm ve diğerleri 2004, Mouzin ve diğerleri 2004, Mitchell ve diğerleri 2012) [EB1]. Bu durum kedilere yapılan temel aşılar için geçerli olmayabilir.
Son yıllarda ortaya çıkan “tek bir sağlık” kavramı, aşılama alanını da etkilemiştir. Enfeksiyona bağlı hastalıkların; tıp, veterinerlik ve çevre sağlığından sorumlu birimlerle birlikte ele alınması rasyonel bir yaklaşımdır ve maliyet düşürme açısından önemlidir. Ayrıca insanlarda yeni ortaya çıkan enfeksiyonların büyük bir kısmı vahşi veya evcil hayvan kaynaklı olarak türemiştir(Gibbs 2014) . WSAVA da “tek bir sağlık” kavramını , bu alanda bir komite kurarak ele almıştır ( Day 2010). Bu komitenin VGG ile faaliyetleri hayvanlardan( köpeklerden) insanlara geçen kuduz ve leishmaniosis hastalıklarında kesişir.
Kedi ve köpeklerin aşılanmasında dikkate alınması gereken diğer bir konu da, her hayvan üzerindeki ilaç ya da aşı yükünü mümkün olduğunca azaltmaktır. Bu yolla bir yandan aşının, muhtemel yan etkileri azaltılmış; öte yandan hayvan sahibi üzerindeki hem zaman hem de ekonomik açıdan olumsuz etki azalmış olur, veterinerler de doğrulanmamış tıbbi yollara başvurmamış olur. Bu nedenle, bu kılavuzda her hayvanın aşılama gerekliliğiyle ilgili akılcı analizler yapılmıştır ve aşılar temel ve temel olmayanlar diye ikiye ayrılmıştır. Bu sınıflandırma, bilimsel kanıtlara ve kişisel deneyimlere dayandırılmıştır (Day ve diğerleri 2012). Aşıların sınıflandırılmasının yanısıra, aşıların koruma sürelerinin daha uzun hale getirilmesi, gereksiz aşı uygulamalarından kaçınılması ve dolayısıyla aşı güvenilirliğini arttırılması hedeflenmektedir. Bu iki değişiklik, veterinerlerin bakış açılarında bir farklılık oluşturmuştur ve artık kabul edilen kurallar arasına yerleşmeye başlamıştır. (5)
Elinizdeki bu kılavuz, hayvanlarını veterinere aşı için götürmeye istekli ve maddi imkanları buna yeterli olan kedi ve köpek sahipleri ele alınarak hazırlanmıştır. VGG, her ülkede bu konuda daha az hassas hayvan sahipleri olduğunun bilincindedir. Ayrıca, bazı ülkelerdeki ciddi boyuttaki hem ekonomik hem de sosyal baskıların aşılama prosedürünün kayıt altına alınmasında olumsuz yönde etkili olduğunu biliyoruz. VGG, bir hayvanın hayatında sadece bir kez aşılanabileceği bir durumda, bunun bağışıklık sisteminin yeterince geliştiği bir erginliğe ulaştığında, yani 16 haftalıkken veya sonrasında yapılmasını tavsiye eder.
VGG aynı zamanda barınak ortamında aşı yapmayı da ele almıştır. Bu kılavuz, yüksek etkileşime açık bu hayvanlar için en ideal korumayı sağlayan öneriler içermektedir. VGG aynı zamanda bu barınakların kısıtlı ekonomik imkanlarının olduğunun bilincindedir. Barınaklarda uygulanacak minimum aşılama protokolü, bu hayvanların barınağa almadan önce veya alınması sırasında bir kez temel aşıların uygulanması şeklinde olacaktır.
Bu kitapçık kedi ve köpek aşılanmasında mevcut sorunları ele almayı hedeflemekte, veterinerlere uygulanabilir yollar göstererek, bu hayvanlar için aşılamanın mantık çerçevesinde yapılmasını sağlamayı hedeflemektedir. VGG’ nin en önemli mesajı şudur:
Bütün hayvanları temel aşılarla aşılamalıyız, temel olmayan aşılar da gerekmedikçe yapılmamalıdır. (6)
AŞI ÇEŞİTLERİ
Aşılar enfeksiyon oluşturanlar ve oluşturmayanlar diye ikiye ayrılır.
Kedi ve köpeklerde kullanılan ve enfeksiyon oluşturan aşıların büyük çoğunluğu öldürücülüğü azaltılmış virüsler içerir (değiştirilmiş canlı virus (modified live virus)-MLV veya seyreltilmiş aşı). Organizmalar canlı ve bozulmamıştır. Düşük derecede enfeksiyon oluşturarak bağışıklık oluşmasını sağlarlar. Hayvanda herhangi bir hastalıklı doku oluşturmadan ve enfeksiyon belirtisi göstermeden çoğalırlar. Canlı aşılar, parenteral yolla uygulandığında bağışıklığı daha etkin bir şekilde sağlarlar. Sıvısal ve hücresel bağışıklık daha güçlü olur. Bazı canlı aşılar direkt olarak mukoza yoluyla uygulanırlar ( burun içi veya ağız yoluyla ) ve bu yolla daha efektif bir mukozal koruma oluştururlar. Anneden geçen antikorlardan yoksun bir hayvana canlı aşıyı bir doz uygulamak korumayı sağlar.
Canlı olmayan aşılar, (öldürülmüş veya inaktif aşılar da denir, çıplak DNA aşıları da içerir) inaktif hale getirilmiş ancak antijenlere dokunulmamış virus veya organizmalar, doğal veya sentetik antijenlerden oluşturulmuş virus veya organizmalar veya bu antijen kodunu oluşturacak DNA’yı içerir. Canlı olmayan ajanlar; enfeksiyon oluşturmazlar, çoğalmazlar ve bir patolojiye sebep olmazlar, enfeksiyona bağlı bir hastalığın belirtilerini göstermezler. Etkisini arttırmak için genellikle bir adjuvan( katkı) gerektirirler ve genellikle koruma oluşturması için birkaç doz uygulama gerekir (yetişkin bir hayvanda bile). Canlı olmayan aşılar parenteral yoldan uygulanır. Daha düşük düzeyde hücresel ve sıvısal( hümoral) bağışıklık oluştururlar. Canlı aşılarla karşılaştırıldığında koruma süreleri daha kısadır.
KÖPEKLERDE AŞI
KÖPEKLERE BİREYSEL BAZDA AŞI YAPILMASI
Tablo-1’de temel ( önerilen ) ve temel olmayan ( isteğe bağlı) aşılar ve önerilmeyen aşılar yer almaktadır. VGG temel aşıyı dünyadaki tüm köpeklere yapılması gereken aşılar olarak tanımlamaktadır. Köpeklere hayat boyunca koruma sağlanması için aşıların önerilen aralıklarda yapılması gerekmektedir. Köpekler için temel aşılar, CDV, CAV tip1 ve tip2 ve CPV2 ve değişik türlerine karşı koruma sağlayan aşılardır. Bazı ülkeler bu sayılanlara ek olarak başka aşıları da zorunlu kabul edebilmektedir. Bu duruma örnek olarak kuduz aşısını gösterebiliriz. Kuduz riskinin olduğu yerlerde, insanları ve köpekleri bu riske karşı korumak için bu aşı o bölgedeki tüm köpeklere rutin olarak uygulanmalıdır. WSAVA, 2030 itibariyle bu hastalığın tamamen yok edilmesi için “tek bir sağlık komitesine” ve International Organisation for Animal Health (OIE)’e destek olmaktadır (Anon 2013b). Birçok ülkede evcil hayvanların uluslarası seyahatinde kuduz aşısı yasal bir gerekliliktir.
Temel olmayan aşılar, yapılan risk fayda (aşı olmama riskine karşı, aşı olup yan etkilerin gelişme riski, buna karşı bağışıklık gelişmesi faydası) analizine göre belirlenen ve coğrafi ve hayat şartlarına bağlı olarak yapılması uygun görülen aşılardır. Önerilmeyen aşılarsa kullanılmasında herhangi bir bilimsel dayanak bulunmayan aşılardır.
YAVRU KÖPEKLERE YAPILACAK AŞILAR
Çoğu köpek hayatının ilk günlerinde anneden geçen antikorlarla (MDA) korunurlar. Bu bağışıklık çoğu yavruda 8-12. haftalarda azalma gösterir ve aşıya hazır hale gelirler. Düşük MDA’lı yavrular aşıya cevap verebilecek güçtedirler ve daha önce aşılanabilir. Yüksek titrede MDA taşıyan yavrular 12. haftadan önce aşıya cevap veremezler (Friedrich & Truyen 2000) [EB1]. Bu nedenle sadece bir tane aşı programı tüm vakaları kapsamaz. VGG temel aşıya ilk olarak 6-8 haftalar arasında başlamayı ve her 2-4 haftalık aralıklarla 16. hafta ve sonrasına kadar devam etmeyi önermektedir. Bu nedenle bir yavruya yapılacak temel aşı sayısı, aşıya başlama yaşıyla ve seçilen aşılama aralıklarıyla belirlenecektir. Mümkün olan aşılama programı tablo 5’ te gösterilmiştir. Bu öneriye göre, eğer aşıya 6.-7. haftalarda başlandıysa, 4 haftalık aralıklarla 4 temel aşı yapılacaktır. 8.-9. haftada başlanan bir aşı programında 4 haftalık aralıkta 3 temel aşı yapılacaktır. (6)
Buna karşın, çoğu aşının prospektüsü başlangıçta 2 doz temel aşı uygulamasını önermektedir. Bazı ilaçlar da 10. haftada bitirmek üzere ruhsatlanmıştır: 2 doz temel aşının 2. dozu 10 haftalıkken yapılır. Bunun altında yatan neden, enfeksiyon riskini azaltıp yavru köpeklerin erken sosyalleşmesini sağlamaktır. VGG erken sosyalleşmenin köpeklerin davranışları üzerindeki olumlu etkisini kabul etmektedir(Korbelik ve diğerleri 2011, AVSAB 2008) [EB1]. Yavru köpekler eğitime katılacaksa, gerekli önlemler alınmalı, köpeğin bulunduğu yerdeki diğer köpeklerin sağlıklı ve tam aşılı olduğundan emin olunmalıdır. Bu eğitim veteriner klinikleri dışında bir yerde yapılmalıdır. Eğer veteriner kliniğinde yapılacaksa, yerler her dersten önce temizlenip dezenfekte edilmeli, seçilen yer aşı ve hastalık durumları bilinmeyen köpeklerin yoğun olarak bulunduğu veya tedavisinde kullanılan bir yer olmamalıdır. Yakın bir zamanda ABD’de yapılan bir araştırma sonucunda, aşılı yavrular eğitime katıldığında bunlar için minimum düzeyde CPV2 riski bulunduğu görülmüştür (Stepita ve diğerleri 2013). VGG temel aşı serisinin sonuncu uygulamasının 16. hafta ve sonrasında yapılmasını önermektedir[EB1].
Yavru köpeklere yapılan aşıların önemli bir parçası da, geleneksel olarak 12. ayda veya ilk aşılardan 12 ay sonra yapılan tekrar aşısı ya da booster aşılarıdır. Bu aşının temel amacı, daha önce yapılan aşıların herhangi biri başarısız olduysa, bağışıklığı oluşturmaktır. Eskiden, bu aşının yapılmasında 12. ayın seçilmesinin nedeni, aynı zamanda hayvanın yıllık sağlık kontrolünün yapılmasını da sağlamaktı. Bu durum eğer yavruya yapılan aşılardan biri tutmadıysa, 12. aya kadar hastalıklara açık olduğu anlamına gelmektedir. VGG bu uygulamayı ele almış ve ve veterinerlere yapılacak tekrar aşıları için 26 ve 52. Haftalar arasını önermiştir. En uygun zaman 26. Haftadır. Köpek sahipleri bunun nedenini kesinlikle anlamadır. Tablo 5’te belirtildiği gibi, böyle bir protokol uygulamak, yavru 6-7 haftalıkken aşıya başlanmasını ve ilk 6 ayda 5 temel aşı için veteriner ziyaretini gerektirmektedir. Temel aşılarda 26. haftada yapılan tekrar aşısından (booster) sonra en azından 3 yıl boyunca başka bir temel aşı gerekmeyecektir. 26. haftada yapılacak tekrar aşısı, hayvan 1 yaşında veya 16 aylık olduğunda yapılması gereken ilk yıllık sağlık kontrolünü aksatmak anlamına gelmemelidir. Çoğu veteriner hayvan iskeleti erişkin bir hale geldiği dönemde sağlık kontrolü yapmaya olumlu yaklaşmaktadır.
YETİŞKİN KÖPEKLERE TEKRAR AŞISI YAPILMASI
MLV temel aşılarına cevap veren köpeklerin birkaç yıl boyunca güçlü bir bağışıklık sistemi oluşur (bağışıklık hafızası) (Bohm ve diğerleri 2004, Mouzin ve diğerleri 2004, Schultz 2006, Mitchell ve diğerleri 2012) [EB1]. 26. hafta veya 52. hafta tekrar aşılarını takip eden aşılar en az 3 yıllık sürelerde yapılır.
Üzerinde durulması gereken nokta bu 3 yıllık aşı dönemlerinin genellikle cansız temel aşılara ( kuduz istisnasıdır) ve temel olmayan aşılara ve özellikle bakteri antikorları taşıyan aşılara uygulanmamasıdır. Bu nedenle Leptospira, Bordetella and Borrelia (Lyme hastalığı) aşıları ve parainfluenza virusu bileşenleriyle güvenilir bir bağışıklık sağlamak için daha sık aşı gerektirir (Ellis & Krakowka 2012, Klaasen ve diğerleri 2014, Ellis 2015, Schuller ve diğerleri 2015) [EB1].
Bu sebepten ötürü, yetişkin bir köpek, bu kitapçığa göre her yıl aşılanabilir. Ama bu aşıların içeriği her sene değişebilir. Temel aşılar 3 senede bir yapılırken, temel olmayan aşılar her sene yapılabilir. VGG bazı ülkelerde karma yapılı hem temel hem de temel olmayan aşıları içeren ürünlerin mevcut olduğunun bilincindedir. VGG üreticileri temel ve temel olmayan aşılardan karma aşı üretmeme konusunda teşvik etmektedir (7) (Mitchell ve diğerleri 2012).
Yavruyken, 26. hafta veya 52. hafta aşıları da dahil olmak üzere tüm aşıları tam olarak yapılmış bir yetişkin köpek, eğer bu dönemde aşılanmazsa, sadece bir doz MLV ile bağışıklık sistemi güçlendirilebilir (Mouzin ve diğerleri 2004, Mitchell ve diğerleri 2012) [EB1]. Aynı şekilde, aşı geçmişi bilinmeyen ve sahiplenilen bir köpeğe ( veya 16 haftadan büyük bir yavruya) bir doz MLV yapılması bağışıklığını korumak için yeterlidir. Çoğu aşı prospektüsü bu şartlar altında köpek veya yavruya 2 aşı yapılmasını salık verse de, bu uygulamayı destekleyen bilimsel veriler mevcut değildir ve bağışıklığın temel prensiplerine karşıttır.[EB4]. Temel olmayan aşıların yetişkin köpekte 2 doz gerektirdiğini yeniden vurgulayalım.
Köpeklere yapılan kuduz aşılarıyla ilgili önemli bir nokta bulunmaktadır. VGG, yayılma riski olan ülkelerde, kuduz aşısı zorunlu olmasa da veterinerler tarafından mutlaka müşterilerine önerilmesini tavsiye etmektedir. Yeniden aşılama dönemleri genellikle yasalarla belirlenir. Uluslarası düzeyde kullanılan mevcut cansız kuduz aşısının koruma süresi 1 yıl olarak ruhsat almıştır; bu nedenle yıllık tekrarlar gerektirir. Aynı ürün, şu anda birçok ülkede 3 yıllık koruma süresine sahiptir. Buna rağmen bazı ülkelerde, yasal düzenlemeler ilacın ruhsat süresini dikkate almamaktadır veya ruhsattaki süre veya yasa da değiştirilmemiştir. Bazı ülkelerin yerel olarak ürettiği ve 1 yıllık koruma süresi taşıyan kuduz aşıları bulunmaktadır. Bunların koruma süreleri güvenilir şekilde 3 yıla kadar uzatılamaz. Veterinerler yasal düzenlemeleri dikkate almalı, dernek ve oluşumlar yasal düzenlemelerin bilimsel kanıtlara uygun hale getirilmesi için çalışmalar yapmalıdır.(8)
Köpeklere yapılan aşıların oluşturduğu bağışıklığın serolojik testlerle ölçülmesi
Kılavuzun yayınlandığı 2010 yılından beri serolojik testlerde gelişmeler olmuş, hızlı ve basit test kitlerinin yaygınlığı artmıştır. Bu testler CDV, CAV ve CPV-2’ ye özgü koruyucu antikorların varlığını belirleyebilmektedir. Bu kitler geleneksel laboratuvar testlerini tamamlayıcı niteliktedir (Gray ve diğerleri 2012, Litster ve diğerleri 2012) [EB1]. 2 tür test uygulanmış ve geçerliliği kanıtlanmıştır. Bu testler müşterilerine 3 yıllık aralıklarla yapılacak aşı dışında bir alternatif önermek isteyen veterinerler arasında popüler olsa da, testler bir doz aşıdan daha pahalıdır.
Negatif bir test sonucu, köpekte çok az miktarda veya hiç antikor olmadığını gösterir ve bu durumda yeniden aşı yapılması tavsiye edilir. Sonuç negatif çıkan bazı köpeklerin aslında bağışıklıkları vardır ve yeniden aşılanmaları gereksizdir. Aşı yapıldığı takdirde buna çabuk ve önemli anamnestik (hafızasal) bir cevap vereceklerdir (Mouzin ve diğerleri 2004). Bu köpekler kolaylıkla belirlenemez ve kullanılan test ne olursa olsun eğer sonuç negatifse , antikor yok ve enfeksiyona açık kabul edilmelidir. Buna karşın pozitif sonuçta yeniden aşı gereksizdir.(9)
Köpeklerdeki kuduz hastalığı söz konusu olduğunda, serumdaki antikorlar aynı şekilde incelenmez. Uluslararası evcil hayvan seyahati düzenlemelerine göre, koruyucu kuduz antikorlarının varlığı laboratuvar testiyle belirlenmelidir (0.5IU/ml’den fazla olmalıdır). Kuduz serolojileri sadece belirli laboratuvarlar tarafından gerçekleştirilmektedir.
CDV, CAV ve CPV-2 ile ilgili serolojik testler yavrularda koruyucu bağışıklığın gelişip gelişmediğini takip etmek, yetişkin köpeklerde tekrar aşılarının aralığını belirlemek ve barınaklarda enfeksiyon salgınlarını önlemekte kullanılabilir.
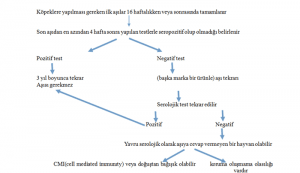
Köpeğiyle ilgili bir yavru köpek sahibi, 16. haftada ilk aşılar tamamlandıktan sonra bunların tutup tutmadığının belirlenmesinin teyidini bu yolla isteyebilir(Şema1). Son aşının yapılmasından en az 4 hafta sonra alınacak bir serum test edilebilir. Bu süre sonunda MDA artık bulunmaz ve en yavaş cevap veren yavrular bile seropozitif olurlar. Pozitif sonuç durumunda yavrunun 26. veya 52. haftalarda yeniden aşılanmasına gerek yoktur. Temel aşılar 3 yıl sonra yapılır. Sonuç negatif olduğunda bu yavrular yeniden aşılanmalı ve test tekrar edilmelidir. Eğer sonuç yine negatifse, yavru aşılara cevap vermiyor anlamına gelir; koruyucu bağışıklık gelişmiyordur.
Antikorları test etmek yavrunun bağışıklık sisteminin aşı antikorlarını kabul edip etmediğini görmenin tek yoludur. Aşının yavruda işlememesinin bir çok sebebi vardır:
1. MDA aşıdaki virusu etkisizleştirir. Bu en sık görülen nedendir. Eğer son aşı 16 haftalıkken veya daha sonrasında yapılırsa, MDA seviyesi azalır (Friedrich & Truyen 2000) [EB1] ve bir çok yavruda aşı başarılı olup bağışıklık geliştirir.
2.Aşı zayıf derecede bağışıklık meydana getirir -zayıf derecede immünojeniktir.
Zayıf bağışıklık, aşının geliştirilmesinden uygulanmasına kadar birçok faktöre bağlı olarak oluşabilir. Mesela, bir virus türü, geçiş öyküsü ve bir üretim serisindeki üretim hataları aşının başarısız olmasına neden olabilir. Aslında, bu etkenler büyük ve iyi kurulmuş ilaç firmalarında nadiren görülür. Bu ilaçlar kullanıma sunulmadan önce etkinlikleri ilgili kurumlar tarafından sıkı bir şekilde kontrol edilir. Üretim sonrası, uygunsuz depolama veya taşıma( bozulmuş soğuk zincir) veya uygulama( dezenfektan kullanımı) hataları MLV aşının başarısını olumsuz etkiler. VGG bu tarz sorunların bazı ülkelerde olabileceğini düşünerek Tablo-6’ da bu konu üzerinde durmuştur.
3. Hayvan zayıf bir şekilde cevap vermektedir( bağışıklık sistemi aşıdaki antijenleri tanımamaktadır).
Eğer bir hayvan tekrarlanan aşılara antikor cevabı veremiyorsa, genetik olarak cevap vermeyen olarak sınıflandırılmalıdır. Çünkü bağışıklık sisteminin cevap verip vermemesi birçok türde genetik olarak kontrol edilir. Bazı köpek türlerinin zayıf cevap veren türler olduğundan şüphelenilmektedir. 1980’ lerde doberman ve rottweilerlara yapılan CPV2 aşılarında oluşan hassasiyetin ( aşı geçmişleri dikkate alınmaksızın) cevap vermeyen ırklara bağlı olduğuna inanılmıştır(Houston ve diğerleri 1994) [EB4]. Bu durum kanıtlanmamıştır. Günümüzde ABD’de bu 2 ırkın diğer ırklardan cevap vermeme bakımından herhangi bir farkı tespit edilmemiştir. Büyük ihtimalle CPV2 enfeksiyonuna bağlı olan bu genetik özellikler yok olmuştur. Bu ırklardan bazı hayvanlar, başka antijenlere zayıf cevap veren hayvanlar olabilir. Örneğin İngiltere ve Almanya’da CPV2 aşısına rotweilerların [EB3] cevap vermediği görülmüştür. Yakın zamanda yapılan araştırmalar bu ırkın kuduz aşısı sonrasında da uluslararası seyahat için gerekli titre sayısına ulaşmada yetersiz kaldığını göstermektedir (Kennedy ve diğerleri 2007) [EB1]. Yapılan tahminlere göre, köpeklerde CDV aşısına cevap vermeme 5000’de 1, CAV ye cevap vermeme 100 000’de 1, CPV2 ye cevap vermeme de 1000’ de 1’ dir[EB4]. (10)
Bağışıklık(koruma) süresini belirlemede kullanılan serolojik testler
Antikor testleri temel aşıların koruma sürelerini göstermede kullanılabilir. CDV, CPV-2 CAV-1 ve CAV-2 gibi aşılara karşı oluşan koruyucu antikorların çoğu köpekte birkaç yıl korunduğu bilinmektedir ve bu gözlemi çok sayıda deneye dayalı araştırma desteklemektedir(Bohm ve diğerleri 2004, Mouzin ve diğerleri 2004, Schultz 2006, Mitchell ve diğerleri 2012) [EB1]. Bu nedenle antikorun eksik olduğu durumlarda,( hangi serolojik test kullanılırsa kullanılsın) , bazıları bağışıklık hafızası tarafından korunsa da, tıbbi bir neden bulunmadıkça köpekler yeniden aşılanmalıdır.
Temel olmayan aşılardan sonra yapılacak serolojik testlerle antikorların belirlenmesi faydalı bir uygulama değildir, çünkü bu antikorlar serumda kısa süre kalırlar. Ayrıca bu aşılar için serumdaki antikorlarla bunların sağladığı koruma arasında düşük bir korelasyon vardır.( örneğin leptospira ve köpek parainfluenzası) (Hartman ve diğerleri 1984, Klaasen ve diğerleri 2003, Ellis & Krakowka 2012, Martin ve diğerleri 2014) [EB1].
VGG günümüzde bu tür serolojik testlerin görece pahalı olabileceğini kabul etmektedir. Buna rağmen kanıta dayalı veteriner hekimlik prensiplerine göre antikor seviyesini belirlemeye yönelik bir test yapmak(yetişkin ve yavru köpeklerde), (daha güvenli ve ucuz olan aşı yapmaya göre) tavsiye edilmektedir. (9)
PASİF BAĞIŞIKLIK
Aşı ya da aktif bağışıklık enfeksiyonel hastalıklara karşı koruma sağlasa da, birçok ülkede enfeksiyonel hastalık tedavisinde pasif bağışıklık kullanılmaktadır.
Virüs enfeksiyonları hücresel ve hümoral bağışıklığa neden olsa da, asıl olarak antikorların cevap vermesi viral yükün azalmasına ve iyileşmeye neden olur. Çoğu viral enfeksiyonda, antikor seviyesi koruma seviyesiyle orantılıdır. Viremia sırasında, önceden varolan veya enjekte edilen antikorlar, ergin viruslerin( virion) partiküllerine bağlanıp, enfektivitelerini etkisiz hale getirir ve onları yok etmek için hazırlar. Pasif bağışıklıkta kullanılan çoğu serum veya immunoglobulin preparatları deri altına enjekte edilirler( çünkü başka hayvan türlerinden elde edilmişlerdir) ve dolaşıma çabucak katılırlar. Beklenen şekilde, plazma ve serumun damar içi enjeksiyonları da iyi bir sonuç verirler. Kuduz bir hayvan tarafından ısırılma gibi lokal enfeksiyonlarda, sonradan yapılan prohylaxis antikorların bir işe yaramadığı tıpta ispatlanmıştır. İnsanlar için olan ve kuduza bağışık hale getirilmiş globulin ilk gün verildiği takdirde hızlı bir koruma sağlar. Hazırlanan karışım, kuduz aşısının yapıldığı alana uzak bir yere, kas içi olarak uygulanır.
Evcil hayvanlarda koruyucu aktif bağışıklık oluşturmak en çok uygulanan yöntemdir. Serum prophylaxis terapisi nadir durumlarda uygulanır,( örneğin köpekte veya kedide gençlik hastalığı varsa veya bir salgın hastalık varsa) bu durumlar için hala ABD, Almanya, Çek Cumhuriyeti, Slovakia, Rusya ve Brezilya’ da serum ve immunoglobin üretimi yapılmaktadır. Preparatlar aynı hayvan türünden veya farklı türlerden (örneğin at) hazırlanıp polivalan çok değerli haldedir( birçok viruse karşı etkili) serum şeklindedir veya immunoglobülin fraksiyonudur.
Bu tarz ürünlerin varlığına rağmen, VGG bunların dikkatli ve ölçülü kullanımını önermektedir. Sadece dikkatli bir durum değerlendirilmesi yapıldıktan sonra kullanılmalıdır. CDV hastalığının bir köpek barınağında görülmesi halinde, bütün köpeklere CDV aşısı yapılması, immun serum uygulamasına göre daha güvenli ve etkin bir tedavi olacaktır. Bakınız tablo 7 (Larson & Schultz 2006) [EB1]. Böyle bir durumda, daha önceleri MLV aşılarının, deri altı veya kas içi yerine damar içi enjeksiyon şeklinde yapılması önerilmekteydi (offlabel uygulama). Ancak damar içi uygulamanın deri altı veya kas içi uygulamaya göre daha hızlı veya etkin olduğunu gösteren kanıtlar son derece azdır.
CDV aşısının belirtilen bu yollardan herhangi biriyle uygulanması halinde, aşı hastalığın çok şiddetli seyretmesine veya ölüme hemen veya çok kısa sürede engel olacaktır. Bu durumda, aşı enfeksiyonu engellemez, ancak şiddetli seyrine (özellikle nörolojik hale gelmesine) engel olur; böylece hayvan hayatına devam edebilecek ve hayatı boyunca bağışıklık kazanmış olacaktır.
Yakın zamanda yapılan araştırmalar, kedi barınağında FPV enfeksiyonu salgın hale gelirse veya köpek barınağında CPV-2 hastalığı görülürse, klinik bulguların görülmesinin ardından immun plazma verildiğinde hastalık veya ölüm görülme oranlarının azalmadığını göstermiştir (Bragg ve diğerleri 2012) [EB1]. Buna rağmen bu çalışma, az miktarda immun plazma (12 ml) verildiği için eleştirilmiştir. Normalde araştırmacılar ve uygulayıcı hekimler tarafından çok daha yüksek dozlarda plazma verilmektedir, bu dozların da etkin olduğu görülmüştür (Dodds 2012) [EB4].En yüksek düzeyde fayda sağlayabilmek için, immun serum ve plazma, enfeksiyondan hemen sonra ancak klinik bulgular görülmeden önce verilmelidir. Bu durumda yüksek titreli serum gereklidir ve immun serum ve plazma enfeksiyonun ilk 24 -48 saatinde verilmelidir. Serum ve plazma oral yolla değil, parenteral yolla verilmelidir. Oral yolla uygulama, hastalık başlamadan dahi yapılsa hiçbir fayda sağlamaz. (11)
Barınaklardaki en büyük sorun, kullanılan ilaçların maliyetidir. Barınaklarda uygulanan alternatif bir yolsa, yakın zamanda aşılanmış ve hastalığı atlatmış hayvanlardan serum ve plazma toplamaktır. Bu yolu uygulamanın da bazı riskleri vardır. Örneğin serumlar kanla geçebilen patojenler içerebilir(haemoparasites ve kedi retro virusü) . Serolojik test uygulamak barınak ortamında salgın hastalıklara engel olmada etkili bir yoldur ( bakınız tablo7)
Kedilerde aşıların yapılabileceği yerler
Enjeksiyon bölgesi sarkomu. Aşılar genellikle enjeksiyon yoluyla yapılan ilaçlar olduğundan, kedilerde enjeksiyona bağlı tümörlere neden olabilirler. Bu nedenle adjuvanlı FeLV ve kuduz aşılarının uygulanması sırasında özellikle dikkat edilmelidir (Kass ve diğerleri 1993). FISS (feline injection site sarcoma) bir çok araştırmanın konusu olmuştur (Martano ve diğerleri 2011, Srivastav ve diğerleri 2012, Ladlow 2013, Hartmann ve diğerleri 2015). Güncel araştırmalardan bazılarının sonuçlarına göre, FISS’ in sebebi açıklanamasa da, günümüzde bunun sebebi olarak, lokal olarak mezenkimal hücrelerindeki kronik enflamasyonun kötü bir değişim geçirmesi gösterilir. (14)
Bu prosesin genetik temelleri vardır. Deri altına yapılan çoğu enjeksiyon( aşı da dahil) geleneksel olarak kedilerin interskapular bölgelerine uygulanmaktadır. Genellikle FISS de bu bölgede gelişmektedir. Bu tümörlere cerrahi yoldan müdahale edilmesi gerekir, bunun yanısıra yardımcı tedaviler de uygulanabilir (Martano ve diğerleri 2011, Ladlow 2013).
Kuzey Amerika’da bu soruna çözüm olarak önerilen protokolde, yüksek riskli kabul edilen adjuvanlı 2 aşının 2 farklı anatomik bölgeye yapılmasının FISS söz konusu olduğunda cerrahi müdahaleyi kolaylaştırıldığı düşünülmektedir. Bunun yanısıra, FeLV aşısının distal sol arka bacağa, kuduz aşısının da distal sağ arka bacağa yapılması önerilmiştir. Bu uygulamalar güncel AAFP kitapçığının içinde de bulunmaktadır (Scherk ve diğerleri 2013). Bu kitapçıkta ayrıca, 3 temel aşının da, distal ön bacağa yapılmasını önerilmektedir. Bir araştırma bu uygulamayı ve sonuçlarını ele almıştır (Shaw ve diğerleri 2009). Araştırmada, FISS’in anatomik dağılımı bu önerinin yapıldığı dönem ve uygulama sonrası dönem bakımından incelenmiştir. Araştırma sonuçları, interskapular alanlardaki tümörlerde anlamlı bir düşüş, ancak sağ bacaklardaki tümörlerde artış göstermiştir. Ayrıca, vücudun farklı bölgelerinde birlikte oluşan tümörlerde de artış görülmüştür. Sağ arka bacakla, sağ lateral abdomende görülen tümörler eskiden % 12.5 iken uygulamadan sonra % 25’e yükselmiştir. Sol arka bacakla, sol lateral abdomende görülen tümörlerde ise % 11.4’ten %13.8 e yükselmiştir. Bu da distal arka bacağa enjeksiyon yapmanın zorluğuna ve abdominal bölgelerin kazayla enjeksion yapılmasına bağlanmıştır. Bu öneriler, Kuzey Amerika dışında sıkça uygulanmamaktadır.
Güncel bir araştırmada, FPV ve kuduz aşılarını kedilerin kuyruğuna uygulamanın etkin sonuçlar verdiğini göstermektedir (Hendricks ve diğerleri 2014). Sahipsiz yetişkin kedilere üçlü MLV temel aşıları yapılmıştır. Canlı olmayan kuduz aşısı ise, kuyrukta daha önce uygulanan aşının 2 cm yanına uygulanmıştır. Bütün kedilerde FPV’ ye karşı serokonversiyon oluşmuştur. Kuduz aşısı ise bir kedi dışında hepsinde tutmuştur. Bu küçük araştırma kuyruğa yapılan aşıların tüm kedilerde iyi tolere edildiğini göstermektedir. 2010 yılındaki kitapçıkta, WSAVA, bir alternatif sunmuştur. Bu alternatifte, lateral göğüs veya daha iyisi lateral abdomen derisine yapmayı önermiştir. Kuyruğa yapılan aşı, distal bacaklara veya lateral vücut bölümlerine yapılan aşılara göre daha güvenli gözükse de daha fazla araştırma gerektirmektedir.
Bu konu karmaşık ve tartışmalı olsa da, uygulayıcı hekimler hangi yaklaşımın kendilerine daha uygun olduğuna karar vermelidirler.
Aşılar tarafından sağlanan koruma, FISS riskine göre daha önemlidir. Yapılan aşılardan FISS olma olasılığı 5000 ila 12500 de birdir (Gobar and Kass 2002, Dean ve diğerleri 2013).
Adjuvanlı olmayan aşılar kedilerin herhangi bir bölgesine uygulanabilir.
- Aşılar veya diğer enjeksiyonlar kedilerin intraskapular bölgelerine yapılmamalıdır.
- Aşılar, özellikle adjuvanlı ilaçlar deri altı bölgelere yapılmalıdır. Kasiçi olmamalıdır.
- Aşı yapılacak alanlar, FISS söz konusu olduğunda, nispeten kolay ameliyat edilebilecek bir bölge olması gözönünde bulundurularak, aynı zamanda aşı yapan kişinin güvenliği de dikkate alınarak belirlenmelidir.( örneğin kediyi tutarken yanlışlıkla enjeksiyonu kendine yapma riski)
- Aşılar her seferinde farklı bir bölgeye yapılmalıdır. Bu da aşı kartına bir şemayla işlenmelidir. Bu alanlar her seferinde değiştirilmelidir. Öte yandan yapılacak diğer bir uygulama, bir yıl boyunca tüm aşıları bir tarafa yapmak ertesi sene de diğer tarafa yapmaktır.
- VGG FISS vakalarının ve aşının yan etkilerinin ilgili makamlara ve aşı üreticisine bildirilmesini tavsiye etmektedir.
Serolojik testler
Kılavuzun yayınlandığı 2010 yılından beri serolojik testlerde gelişmeler olmuş, hızlı ve basit test kitlerinin yaygınlığı artmıştır. Bu testler FPV, FCV ve FHV-1’ ye özgü koruyucu antikorların varlığını belirleyebilmektedir. Bu testler yayınlanmış seri araştırmalarla desteklenmiştir (DiGangi ve diğerleri 2011, Mende ve diğerleri 2014) [EB1]. FPV’ye karşı koruyucu antikorların varlığını belirlemede kullanılmaktadır. Bu antikorlarını varlığı ve enfeksiyona dayanıklılık arasında sıkı bir ilişki bulunmaktadır(Lappin ve diğerleri 2002) [EB1]. FPV test kitleri hemaglutinasyon baskılama (haemagglutination inhibition) testiyle karşılaştırıldığında% 89 oranında özgün, % 79 oranında hassas olduğu (Mende ve diğerleri,2014) ve başka bir araştırmada % 99 özgün, % 49 hassas olduğu (DiGangi ve diğerleri, 2011) görülmüştür. Negatif test sonucu, kedide çok az antikor olduğunu veya hiç antikor bulunmadığını gösterir. Ancak bazı negatif sonuçlu kediler bağışıktır ve yeniden aşılanmalarına gerek yoktur. Buna karşın pozitif bir sonuçta yeniden aşılanmaya gerek yoktur.
Serumla dolaşıma giren antikorlar ve FCV ve FHV-1’ e karşı koruma arasındaki korelasyon, lokal mukozal bağışıklık ve hücresel bağışıklık kadar güçlü değildir. Bu nedenle, bir kedide FCV ve FHV- 1 aşılarını izleyen bir test sonucu negatif çıksa da, kedide koruma sağlayabilir (Lappin ve diğerleri 2002) [EB1]. Bu testler daha önce köpekler konusunda bahsedildiği gibi kediler için de kullanılabilir. Yavru kedilerde FCV aşısından sonra korumanın oluşup oluşmadığını görmede, yetişkin kedilerde FPV’ ye karşı bağışıklığı belirlemede ( yeniden aşı yapma kararı vermeden önce) ve barınaklarda FPV salgınlarını önlemede kullanılabilir. Üzerinde durulması gereken diğer bir nokta ise FIV için yapılan antikor testinin hastalığı teşhis etmede kullanılması, FIV’ e olan bağışıklığı ölçmede kullanılmamasıdır. Fakat FIV enfeksiyonundan şüphelenildiği ve FIV aşısının yapıldığı durumlarda, teşhis serolojik farklılık(discriminatory) testlerine dayandırılmalıdır. Özellikle onaylanmış PCR testi kullanılabilir.
Yeni köpek aşılarıyla ilgili güncelleme
2010 yılında WSAVA kılavuzunun yayımlanmasından beri yeni aşılar piyasaya sürülmüştür. Bunlar, oral kullanım için bordetella brochiseptica aşısı (Hess ve diğerleri 2011, Ellis 2015) ve uluslarası kullanıma sürülen leptospira aşılarıdır. Sonuncu aşı çok sayıda, coğrafik olarak geçerli serogroup taşır (Klaasen ve diğerleri 2012, 2014, Wilson ve diğerleri 2013, Schuller ve diğerleri 2015). Bu ürünler tablo 1 de anlatılmıştır.
CIV(Canine Influenza Virus)’ e karşı bir aşı da sadece ABD’ de ruhsat almıştır (Deshpande ve diğerleri 2009, Larson ve diğerleri 2011). Bir arada yaşayan Kuzey Amerikalı köpeklerdae görülen A tipi H3N8 virüsü solunum yolları hastalığının sebebi olarak bulunmuştur (Crawford ve diğerleri 2005, Payungporn ve diğerleri 2008, Castleman ve diğerleri 2010) Ancak başka yerlerde sadece seyrek salgınlar tespit edilmiştir.(Crawford ve diğerleri 2005, Daly ve diğerleri 2008, Kirkland ve diğerleri 2010, Pratelli & Colao 2014, Schulz ve diğerleri). CIV aşısında cansız virusler bulunur ve yavrulara 6 haftalıktan itibaren uygulanmaya başlar. İkinci doz 2 ila 4 hafta sonra uygulanır. Daha sonra yıllık tekrar aşıları yapılır. Bağışıklık 2. dozdan sonra 7 gün içinde oluşur. Bu aşı temel aşı olarak kabul edilmez ve Kuzey Amerika’daki risk altında bulunan köpekler için tavsiye edilir (Anderson ve diğerleri 2013) [EB1]. Yazım aşamasında, ABD’nin Chicago ve Wisconsin bölgelerinde köpeklerde görülen influenzanın bir türü olan H3N2 rapor edilmiş ve bu aşının bir alt tipi piyasaya tedavi için sürülmüştür.
2010 yılında köpeklerdeki malin melonoma karşı ilk immunoterapatik aşı için ruhsat alınmıştır. Bu ilaç insanlardaki tyrosinase geninin plazmidle birleştirilmiş halini içerir( çıplak DNA aşısı) ve yüksek basınçlı transdermal bir enjeksiyon aletiyle uygulanır. Ağız çevresinde melanoma olan köpeklerde ek bir tedavi yöntemi olarak kullanılır ve bu melanoma için hedeflenen antikora bir bağışıklık cevabı oluşturur. Başlangıç düzeyindeki araştırmalar, bu aşının, 2 ila 4. evrelerdeki köpeklerin yaşam süreleri 90 günden 389 güne çıkardığını göstrmektedir(Bergman ve diğerleri 2006). Ama daha güncel araştırmalar, daha az etkisi olduğunu göstermiştir (Grosenbaugh ve diğerleri 2011, Ottnod ve diğerleri 2013) [EB1]. Bu aşı A.B.D.’de olduğu gibi Avrupa’da da mevcuttur, ve sadece belli onkolog veterinerler tarafından kullanılır.
Brezilya’da köpeklerdeki Leishmaniosis için 2 tane ruhsat almış aşı bulunmaktadır. Bu ülkede Leishmaniosis hem insan hem de köpek popülasyonu için önemli bir tehlikedir. Bu aşılardan ilki, Leishmania Donovani’ nin saponin adjuvanlı GP63’ini (aynı zamanda fucose mannose ligand denmektedir; FML) bulundurur. Organizmanın köpekten tatarcık vektörüne geçmesini bloke eden bir antikor bulundurur. Bu yolla Leishmania tatarcığın orta bağırsağına( midgut) bağlanamaz. (Palatnik de Sousa ve diğerleri 2009; Palatnik de Sousa & Day 2011) [EB1]. Bu bağışıklık, araştırmalarda ve epidemiyolojik saha araştırmalarında derinlemesine incelenmiştir. Buna karşın bu ürün piyasadan kaldırılmıştır. İkinci aşı L. Donovaninin saponİn adjuvanının A2 antikorunu bulundurur. Bu aşı, 11 ay boyunca, bulaşıcı hastalığın görüldüğü bir bölgede uygulandığında, FML aşısıyla benzer sonuçlar gösterdiği görülmüştür (benzer serokonversiyon, enfeksiyon ve klinik belirtilerinden korunma ve vektöre iletim). A2 aşısıyla aşılanmış köpekler, daha düşük bir humoral bağışıklık geliştirmiş, ancak yan etkiler daha sık görülmüştür (Fernandes ve diğerleri 2014).
2011’de Avrupa’da Leishmania için bir aşı geliştirilmiştir (Bongiorno ve diğerleri 2013; Moreno ve diğerleri 2013). Bu aşı Leishmania’nın Leismania infantum’un adjuvandaki ekstretuar-sekretuar(boşaltımsal-salgısal)antijenlerini bulundurur. Bu aşı 6 aylıktan itibaren seronegatif köpeklerde 3 haftalık aralıklarla üç doz halinde kullanılır. Bu başlangıç serisinden sonra tekrar aşıları yıllık olarak yapılır. Aşılı köpekler seropozitif hale gelirler. Hücresel bağışıklık da gelişir. Aşı enfeksiyon riskini azaltıp, hastalığın klinik belirtilerini azaltır, ancak insan sağlığı üzerindeki bir etki beklenmemektedir [EB2].
KEDİLERDE AŞI
KEDİLERE BİREYSEL BAZDA AŞI YAPILMASI
Kedilerde temel, temel olmayan ve önerilmeyen aşılarla ilgili bilgiler tablo-3’te verilmektedir. Kedilere uygulanan temel aşılar, FPV( kedi gençlik hastalığı), FHV-1 ve FCV aşılarıdır. Bazı ülkelerde temel olarak kabul edilen aşılardan biri kuduz aşısıdır. Kuduzun yayılma riski olan coğrafi alanlarda, VGG tüm kedilere rutin olarak kuduz aşısı yapılmasını önermektedir. Bazı ülkelerde, kuduz aşısı yasal bir zorunluluktır( kedileri kapsamasa da). Ayrıca, evcil hayvanların uluslararası seyahati için kuduz aşısı gereklidir.
Kedilere uygulanan, FCV ve FHV-1 aşıları, FPV aşısının sağladığı bağışıklığı sağlamaz. Kedilere uygulanan solunum yolları hastalıklarını engelleyici aşıların köpeklerinki kadar güçlü ve uzun süreli olması beklenmemelidir. FCV aşıları farklı türden FCV’lere karşı bağışıklık sağlama amacıyla geliştirilmiştir. Yine de aşılanmış hayvanlarda enfeksiyon ve hastalık görülebilir(Pedersen ve diğerleri 2000, Schorr-Evans ve diğerleri 2003) [EB1].Virulan viruslü enfeksiyona karşı koruyan bir FHV-1 aşısı yoktur. Enfeksiyon görüldüğünde virulan virus gizli hale gelip, daha sonra şiddetli stres görüldüğünde yeniden aktifleşebilir (Richter ve diğerleri, 2009, Maes 2012) [EB1].Yeniden görüldüğünde aşılı hayvanda klinik belirtiler gösterebilir, elverişli hayvanlara geçip onlarda hastalığa sebep olabilir. VGG, yayımlanmış araştırmalara dayanarak düşük risk altındaki kedilere 3 yılda bir FHV-1 ve FCV aşılarının yapılmasını önermektedir. Bu araştırmalar, aşıların kesintili de olsa 7.5 yıl boyunca koruma sağladığını ortaya koymaktadır(Scott & Geissinger 1999). Daha yeni bir araştırma, FHV-1/ FCV aşısının, aşıyı izleyen 3 yılda sağladığı korumanın daha az güçlü ve kısmi olduğunu ortaya koymaktadır(Jas ve diğerleri 2015). VGG yüksek riskli durumlarda, kedilerin yıllık olarak FHV-1/FCV aşılarıyla aşılanmalarını önermektedir. Evde yalnız yaşayan bir kedi düşük riskli olarak kabul edilmektedir. Çok kedinin olduğu bir ortamda yaşayan, dışarıda ve evde yaşayan veya düzenli olarak başka kedilerin kaldığı kedi otellerine/pansiyonlarına giden kediler yüksek riskli olarak kabul edilir. Bu aşıların en kuvvetli koruduğu dönem, aşının yapılmasını izleyen 3 aydır. Bu nedenle, VGG, bu aşıların zamanlamasının kedilerin yüksek riskli bir ortama girmeden öncesine göre ayarlanmasını tavsiye etmektedir(Gaskell ve diğerleri 2007) [EB1]. (12)
FeLV virusüne karşı yapılan aşı, uzmanlar arasındaki tartışma konularından bir tanesidir. VGG, FeLV’ yi temel olmayan bir aşı olarak nitelendirmektedir (Tablo3), öte yandan bu aşının kullanımının hayvanın yaşam biçimi, karşı karşıya olduğu riskler ve o coğrafyadaki enfeksiyonun yaygınlığına bağlı olarak değerlendirilmesini istemektedir. FeLV virüsü başarılı kontrol programları sayesinde artık yaygın değildir. FeLV virusünün yaygın olduğu yerlerde, ev dışına çıkan 1 yaşın altındaki tüm kedilerin aşılanması gerektiği savunulmaktadırlar (Weijer and Daams 1976, Weijer ve diğerleri 1986,1989, Meichner ve diğerleri 2012) [EB1]. Bu aşı, 8 haftalıktan itibaren, 2-4 haftalık aralıklarla 2 doz halinde yapılmalıdır. FeLV aşıları için fayda zarar analizi her zaman yapılmalı ve FeLV negatif kediler aşılanmalıdır. (13)
VGG daha önceki baskılarda tavsiye edilmeyen aşılar statüsünde olan FIV aşısını da ele almıştır. Daha önce tavsiye edilmemesinin sebepleri:
1. Aşının içindeki viruslerin altgrupları ve bu altgrupların farklı coğrafi alanlarda olmasıydı(Hosie ve diğerleri 1995, Dunham ve diğerleri 2006, Yamamoto ve diğerleri 2007, Coleman ve diğerleri 2014, Beczkowski ve diğerleri 2015a) [EB1],
2. FIV enfeksiyonunu teşhis etmede kullanılan antikor testiyle etkileşimi(Hosie & Beatty 2007) [EB1],
3. Sarkoma olma riski bulunan türlere tekrarlanan bir şekilde yapılması gereken bir adjuvanlı aşı olması.( ilk aşamada yapılan 3 doz aşıyı, yıllık tekrar izlemeltedir) (Bennett ve diğerleri 1989, Hosie ve diğerleri 1989, Friend ve diğerleri 1990, Glennon ve diğerleri 1991, Bandecchi ve diğerleri 1992, Hitt ve diğerleri 1992, Ueland and Lutz 1992, Jones ve diğerleri 1995, Hofmann-Lehmann ve diğerleri 1996, Yilmaz ve diğerleri 2000, Lee ve diğerleri 2002, Muirden 2002, Norris ve diğerleri 2007, Gleich ve diğerleri 2009, Ravi ve diğerleri 2010, Bande ve diğerleri 2012, Chang Fung Martel ve diğerleri 2013, Rypula ve diğerleri 2014) [EB1].
VGG dünyanın bazı bölgelerinde, FIV enfeksiyonunun yaygın olduğunu kabul etmektedir. Eskisine göre teşhisi kolaylaştıracak kan testleri ve PCR testleri bulunmaktadır (Arjona et al. 2007, Wang et al. 2010, Morton et al. 2012) [EB1]. Kedi sahiplerinin kedilerini dışarıya bırakmamalarını sağlamak FIV virusune karşı korusa da ( örneğin enfekte bir kedi tarafından ısırılmak), bunu yapabilmek zordur. FIV taşıyan kedilerin, hastalıklarının seyrinde yaşam koşullarının ve bulundukları ortamdaki kedi sayısının önemli olduğunu araştırmalar göstermektedir(Beczkowski et al. 2015b). Bazı araştırmalar bu aşının başarılı sonuçlar verdiğini gösterse de bazıları tersini söylemektedir. Bazı risk altındaki kedi popülasyonları üzerinde aşının faydalı olabileceğini gözönünde bulunduran VGG, bu aşıyı temel olmayan aşılar başlığı altında sınıflandırmıştır.
YAVRU KEDİLERE YAPILAN AŞILAR
Daha önce yavru köpeklerde bahsedildiği gibi, çoğu yavru kedi ilk haftalarda MDA tarafından korunur. Ancak serolojik test yapılmadan, koruma seviyesi, hangi aşamada hastalık riski oluşacağı ve kedinin aşıya nasıl cevap vereceği bilinemez. Bu anneden geçen antikorların seviyesine ve bir batında doğan yavruların MDA alma seviyelerine bağlıdır. Genellikle, 8 ila 12 haftalarda MDA, aktif bir bağışıklık cevabı verecek seviyeye gelir. Öte yandan, düşük MDA’lı yavrular aşıya daha erken cevap verebilir. Yüksek titreli MDA’sı olanlar ise, ancak 12. haftadan sonra cevap verebilirler. VGG bu konudaki araştırmaları gözden geçirmiştir. Bunlara göre, yavru kedilerin üçte birinde, 16 haftalıkken yapılan temel aşıya karşı bağışıklık oluşmaz ve bir bölüm kedide aşıyı etkisiz hale getiren MDA 20 haftalık olana kadar devam eder (DiGangi ve diğerleri 2012, Jakel ve diğerleri 2012). VGG bu araştırmalardan birini sadece 1 ırk tarafından domine edilen sınırlı sayıda kedi popülasyonu üzerinde yapıldığını ve tüm kedi popülasyonuna uygulanabilir olmadığını düşünmektedir.. Öte yandan VGG, temel aşı serilerindeki son aşının zamanını 14 – 16 hafta arasından, 16 hafta ve sonrasına çıkarmıştır [EB1].
VGG yavru kedilere de yavru köpeklere benzer aşı tavsiyelerinde bulunmaktadır. Şöyle ki: 6 ila 8 haftalıkken ilk aşılara başlamak ve 16. hafta veya biraz sonrasına kadar 2 ila 4 haftalık aralıklarla bu aşıları tekrarlamak. Bu nedenle yavru kediye yapılacak temel aşıların sayısı, aşıya başlangıç tarihi ve aşı aralıklarıyla belirlenmiş olacaktır. Mümkün olan aşı takvimi tablo-5 te belirtilmiştir. Sonuç olarak, bu aşı tavsiyelerine uyulduğunda, aşıya kedi 6-7 haftalıkken başlanırsa, 4 temel aşı, 8-9 haftalıkken başlanırsa 3 temel aşı yapılacaktır.
Yavru kedilere yapılan aşıların bir parçası da tekrar aşılarıdır. Bu aşılar geleneksel olarak 12 . ayda veya son aşıdan 12 ay sonra yapılmaktadır. Tekrar aşısının temel amacı, daha önceki yapılan temel aşıların herhangi bir sebep yüzünden tutmaması durumunda, koruyucu bir bağışıklık geliştirmektedir. Bu aşının 12. ayda yapılmasının sebebi, ilk yıllık sağlık kontrolüne denk düşürerek sahibi için uygun hale getirmektir. Bu durum, eğer yavruya yapılan ilk aşılardan biri tutmadıysa, 12. aydaki aşıya kadar hastalıklara açık olduğu anlamına gelmektedir. VGG bu uygulamayı ele almış ve veterinerlere yapılacak tekrar aşıları için 26. ve 52. haftalar arasını önermiştir. Ancak en uygun zaman 26. haftadır. Kedi sahipleri bunun nedenini kesinlikle anlamadır. Tablo 5’te belirtildiği gibi, böyle bir protokol uygulamak, yavru 6-7 haftalıkken aşıya başlanmasını ve ilk 6 ayda aşı için 5 kez veteriner ziyaretini gerektirmektedir. Temel aşılarda, 26. haftada yapılan tekrar aşısından sonra en azından 3 yıl boyunca başka bir temel aşı gerekmeyecektir. 26. haftada yapılan tekrar aşısı, yavru 12 aylık veya 16 aylık olduğunda yapılacak bir sağlık kontrolüne engel teşkil etmemektedir.
Yetişkin Kedilere Aşı Yapılması
MLV temel aşılarına cevap veren kedilerde, aşı tekrarlanmasa da, FPV’ye karşı birkaç yıl boyunca güçlü bir bağışıklık sistemi oluşur (bağışıklık hafızası). FCV ve FHV-1’e karşı bağışıklık ise kısmen olur(Scott and Geissinger 1999, Jas ve diğerleri 2015).VGG düşük riskli yetişkin kedilere MLV aşılarla tekrar aşılarının 3 yıldan daha sık olmayan aralıklarla yapılmasını tavsiye etmektedir.Veteriner yüksek risk altındaki kediler için FPV aşısının 3 yıllık aralıklarla yapılmasını isteyebilir. Ancak FCV ve FHV-1 aşılarını yıllık olarak, kedilerin kedi pansiyonunda kalmalarından hemen önce tekrarlayabilir[EB1]. Üzerinde durulması gereken nokta bu önerilerin genellikle cansız temel aşılara ( kuduz istisnasıdır) ve temel olmayan aşılara ve özellikle bakteriyel antijen taşıyan aşılara uygulanmamasıdır. Bu nedenle Chlamydia (önceki ismi Chlamydophila; Sachse ve diğerleri 2015) ve Bordetella aşılarının kullanımı gerekli görülüyorsa, yıllık olarak tekrarlanmalıdır. Çünkü bu ürünlerin sağladığı koruma sınırlıdır [EB2].
Bu nedenle, bu kitapçığa göre, yetişkin bir kediye her yıl aşı yapılabilir. Ama bu aşıların içeriği seneden seneye değişebilir. Temel aşılar(özellikle FPV) 3 senede bir yapılırken solunum yolları virusleriyle ilgili aşılar riske göre belirlenmekte ve temel olmayan aşılarsa her sene yapılabilmektedir. VGG bazı ülkelerde sadece karma yapılı, hem temel hem de temel olmayan aşıları içeren ürünlerin mevcut olduğunun bilincindedir. VGG üreticileri temel ve temel olmayan aşılardan karma aşı üretmeme konusunda teşvik etmektedir.
Yavruyken, 26 hafta veya 52. hafta aşıları da dahil olmak üzere, FPV, FHV-1 ve FCV aşıları tam olarak yapılmış bir yetişkin kedi, eğer bu dönemde aşılanmazsa, sadece bir doz MLV ile bağışıklık sistemi güçlendirilebilir [EB4]. Aynı şekilde, aşı geçmişi bilinmeyen ve sahiplenilen bir kediye( veya 16 haftadan büyük bir yavruya) bir doz MLV FPV temel aşısı yapılması bağışıklığını korumak için yeterlidir. Buna karşın aşı geçmişi bilinmeyen sahiplenilmiş yetişkin bir kediye 2-4 haftalık aralıklarla 2 doz MLV FHV-1/FCV aşısı yapmak yeterli bağışıklık oluşturacaktır [EB2].
Kedilerde aşıların yapılabileceği yerler
Enjeksiyon bölgesi sarkomu. Aşılar genellikle enjeksiyon yoluyla yapılan ilaçlar olduğundan, kedilerde enjeksiyona bağlı tümörlere neden olabilirler. Bu nedenle adjuvanlı FeLV ve kuduz aşılarının uygulanması sırasında özellikle dikkat edilmelidir(Kass ve diğerleri 1993). FISS(feline injection site sarcoma) bir çok araştırmanın konusu olmuştur (Martano ve diğerleri 2011, Srivastav ve diğerleri 2012, Ladlow 2013, Hartmann ve diğerleri 2015). Güncel araştırmalardan bazılarının sonuçlarına göre, FISS’ in sebebi açıklanamasa da, günümüzde bunun sebebi olarak, lokal olarak mezenkimal hücrelerindeki kronik enflamasyonun kötü bir değişim geçirmesi gösterilir. (14)
Bu prosesin genetik temelleri vardır. Deri altına yapılan çoğu enjeksiyon( aşı da dahil) geleneksel olarak kedilerin interskapular bölgelerine uygulanmaktadır. Genellikle FISS de bu bölgede gelişmektedir. Bu tümörlere cerrahi yoldan müdahale edilmesi gerekir, bunun yanısıra yardımcı tedaviler de uygulanabilir (Martano ve diğerleri 2011, Ladlow 2013).
Kuzey Amerika’da bu soruna çözüm olarak önerilen protokolde, yüksek riskli kabul edilen adjuvanlı 2 aşının 2 farklı anatomik bölgeye yapılmasının FISS söz konusu olduğunda cerrahi müdahaleyi kolaylaştırıldığı düşünülmektedir. Bunun yanısıra, FeLV aşısının distal sol arka bacağa, kuduz aşısının da distal sağ arka bacağa yapılması önerilmiştir. Bu uygulamalar güncel AAFP kitapçığının içinde de bulunmaktadır (Scherk ve diğerleri 2013). Bu kitapçıkta ayrıca, 3 temel aşının da, distal ön bacağa yapılmasını önerilmektedir. Bir araştırma bu uygulamayı ve sonuçlarını ele almıştır (Shaw ve diğerleri 2009). Araştırmada, FISS’in anatomik dağılımı bu önerinin yapıldığı dönem ve uygulama sonrası dönem bakımından incelenmiştir. Araştırma sonuçları, interskapular alanlardaki tümörlerde anlamlı bir düşüş, ancak sağ bacaklardaki tümörlerde artış göstermiştir. Ayrıca, vücudun farklı bölgelerinde birlikte oluşan tümörlerde de artış görülmüştür. Sağ arka bacakla, sağ lateral abdomende görülen tümörler eskiden % 12.5 iken uygulamadan sonra % 25’e yükselmiştir. Sol arka bacakla, sol lateral abdomende görülen tümörlerde ise % 11.4’ten %13.8 e yükselmiştir. Bu da distal arka bacağa enjeksiyon yapmanın zorluğuna ve abdominal bölgelerin kazayla enjeksion yapılmasına bağlanmıştır. Bu öneriler, Kuzey Amerika dışında sıkça uygulanmamaktadır.
Güncel bir araştırmada, FPV ve kuduz aşılarını kedilerin kuyruğuna uygulamanın etkin sonuçlar verdiğini göstermektedir (Hendricks ve diğerleri 2014). Sahipsiz yetişkin kedilere üçlü MLV temel aşıları yapılmıştır. Canlı olmayan kuduz aşısı ise, kuyrukta daha önce uygulanan aşının 2 cm yanına uygulanmıştır. Bütün kedilerde FPV’ ye karşı serokonversiyon oluşmuştur. Kuduz aşısı ise bir kedi dışında hepsinde tutmuştur. Bu küçük araştırma kuyruğa yapılan aşıların tüm kedilerde iyi tolere edildiğini göstermektedir. 2010 yılındaki kitapçıkta, WSAVA, bir alternatif sunmuştur. Bu alternatifte, lateral göğüs veya daha iyisi lateral abdomen derisine yapmayı önermiştir. Kuyruğa yapılan aşı, distal bacaklara veya lateral vücut bölümlerine yapılan aşılara göre daha güvenli gözükse de daha fazla araştırma gerektirmektedir.
Bu konu karmaşık ve tartışmalı olsa da, uygulayıcı hekimler hangi yaklaşımın kendilerine daha uygun olduğuna karar vermelidirler.
Aşılar tarafından sağlanan koruma, FISS riskine göre daha önemlidir. Yapılan aşılardan FISS olma olasılığı 5000 ila 12500 de birdir (Gobar and Kass 2002, Dean ve diğerleri 2013).
Adjuvanlı olmayan aşılar kedilerin herhangi bir bölgesine uygulanabilir.
- Aşılar veya diğer enjeksiyonlar kedilerin intraskapular bölgelerine yapılmamalıdır.
- Aşılar, özellikle adjuvanlı ilaçlar deri altı bölgelere yapılmalıdır. Kasiçi olmamalıdır.
- Aşı yapılacak alanlar, FISS söz konusu olduğunda, nispeten kolay ameliyat edilebilecek bir bölge olması gözönünde bulundurularak, aynı zamanda aşı yapan kişinin güvenliği de dikkate alınarak belirlenmelidir.( örneğin kediyi tutarken yanlışlıkla enjeksiyonu kendine yapma riski)
- Aşılar her seferinde farklı bir bölgeye yapılmalıdır. Bu da aşı kartına bir şemayla işlenmelidir. Bu alanlar her seferinde değiştirilmelidir. Öte yandan yapılacak diğer bir uygulama, bir yıl boyunca tüm aşıları bir tarafa yapmak ertesi sene de diğer tarafa yapmaktır.
- VGG FISS vakalarının ve aşının yan etkilerinin ilgili makamlara ve aşı üreticisine bildirilmesini tavsiye etmektedir.
Serolojik testler
Kılavuzun yayınlandığı 2010 yılından beri serolojik testlerde gelişmeler olmuş, hızlı ve basit test kitlerinin yaygınlığı artmıştır. Bu testler FPV, FCV ve FHV-1’ ye özgü koruyucu antikorların varlığını belirleyebilmektedir. Bu testler yayınlanmış seri araştırmalarla desteklenmiştir (DiGangi ve diğerleri 2011, Mende ve diğerleri 2014) [EB1]. FPV’ye karşı koruyucu antikorların varlığını belirlemede kullanılmaktadır. Bu antikorlarını varlığı ve enfeksiyona dayanıklılık arasında sıkı bir ilişki bulunmaktadır(Lappin ve diğerleri 2002) [EB1]. FPV test kitleri hemaglutinasyon baskılama (haemagglutination inhibition) testiyle karşılaştırıldığında% 89 oranında özgün, % 79 oranında hassas olduğu (Mende ve diğerleri,2014) ve başka bir araştırmada % 99 özgün, % 49 hassas olduğu (DiGangi ve diğerleri, 2011) görülmüştür. Negatif test sonucu, kedide çok az antikor olduğunu veya hiç antikor bulunmadığını gösterir. Ancak bazı negatif sonuçlu kediler bağışıktır ve yeniden aşılanmalarına gerek yoktur. Buna karşın pozitif bir sonuçta yeniden aşılanmaya gerek yoktur.
Serumla dolaşıma giren antikorlar ve FCV ve FHV-1’ e karşı koruma arasındaki korelasyon, lokal mukozal bağışıklık ve hücresel bağışıklık kadar güçlü değildir. Bu nedenle, bir kedide FCV ve FHV- 1 aşılarını izleyen bir test sonucu negatif çıksa da, kedide koruma sağlayabilir (Lappin ve diğerleri 2002) [EB1]. Bu testler daha önce köpekler konusunda bahsedildiği gibi kediler için de kullanılabilir. Yavru kedilerde FCV aşısından sonra korumanın oluşup oluşmadığını görmede, yetişkin kedilerde FPV’ ye karşı bağışıklığı belirlemede ( yeniden aşı yapma kararı vermeden önce) ve barınaklarda FPV salgınlarını önlemede kullanılabilir. Üzerinde durulması gereken diğer bir nokta ise FIV için yapılan antikor testinin hastalığı teşhis etmede kullanılması, FIV’ e olan bağışıklığı ölçmede kullanılmamasıdır. Fakat FIV enfeksiyonundan şüphelenildiği ve FIV aşısının yapıldığı durumlarda, teşhis serolojik farklılık(discriminatory) testlerine dayandırılmalıdır. Özellikle onaylanmış PCR testi kullanılabilir.
BARINAKTA BULUNAN KEDİ VE KÖPEKLERE AŞI YAPILMASI
Hayvan barınağı, sahiplenilmeyi ya da sahipleri tarafından bulunmayı bekleyen hayvanların bulunduğu bir yerdir. Genellikle hayvan barınakları, aşı geçmişleri bilinmeyen rastgele ırk dağılımı olan ve yüksek enfeksiyon riski olan ortamlardır. Her hayvan için ayrı aşı stratejisi olduğu gibi her barınak için de farklı aşı stratejileri bulunmaktadır. İçinde barındırdığı yüksek riskler ve bulaşıcı hastalık olasılığı yüzünden barınakların açık ve net bir aşı stratejileri olmalıdır.
Barınakta uygulanan hekimlik, klinikteki bireysel uygulamalardan farklıdır. Barınakta hastalığın kökünü kurutamama riski bulunmaktadır. Hastalığın yayılma olasılığını yüksek riskli bir ortamda azaltmak ve hastalık bulaşmamış hayvanlar için koruma sağlamak mümkündür. Karmaşık değişkenlerin etkili olduğu bu ortamda, sahiplenilen hayvanların sağlıklı bir şekilde ortamdan ayrılması hedeflendiği gibi, kalan hayvanların da bulaşıcı hastalıklardan korunması amaçlanmaktadır. Bu kitapçıktaki öneriler, sadece barınağa özgü bazı problemleri ele almakta ve aşı ve hastalık kontrolünü incelemektedir.
Tablo 2 ve 4’te barınaklarda uygulanacak aşılarla ilgili bilgiler ve öneriler bulunmaktadır. Güncellenmiş bu kitapçıkta, ,yavru kediler ve köpeklerle ilgili öneriler güncellenmiştir: barınaktaki yavrular 4 ila 6 haftalıkken temel aşı yapılmaya başlanmalıdır. Kaynakların elverdiği durumlarda, aşılar , hayvan 20 haftalık olana kadar 2 haftada bir tekrarlanmalıdır. ABD’de yapılan son çalışmalarda, barınağa gelen kedilerin seropozitif olabileceğini göstermektedir. Eğer barınağa giren bir hayvanın aşı belgelerine ulaşılabiliyorsa ve bu bilgiler karmaşa yaratıyorsa, köpeklere temel aşıların yapılmasına gerek yoktur. Ancak kedilere temel aşılar yapılmalıdır, özellikle fcv ve fhv-1 aşıları yapılmalıdır ki bağışıklık arttırılsın.
VGG barınak ve kedi köpek pansiyonları arasındaki ayrımı yapmaktadır. Bu pansiyonlarda aşıları tam hayvanlar genellikle kısa sürelerde kalırlar( örneğin sahipleri tatildeyken). Bu pansiyonlara hayvan kabulünde her hayvanın temel aşılarının bu kitapçığa uygunluğu mutlaka belgelenmelidir. Köpekler için ayrıca, temel olmayan, solunum yolları enfeksiyonlarına karşı olan aşının aranması da uygun olacaktır. VGG bazı ülkelerde bu pansiyonları düzenleyen yasaların yerel kurumlarca belirlendiğini ve bu düzenlemelerin bu kitapçıkta yazanlarla çatışabileceğini bilmektedir( örneğin aşıların her yıl tekrar edilmesi konusunda ısrar etme). VGG bu kurumların yeni bilimsel verileri dikkate alarak değerlendirmelerini yeniden yapmaları konusunda veterinerlerin ve bunların oluşturduğu sivil toplum kuruluşlarının çalışması konusunda tavsiye vermektedir.
2010 yılında yayımlanan kitapçıktan sonra piyasaya çıkan hızlı ve kolay uygulanabilir serolojik test kitleri, barınaklardaki CDV, CPV ve FPV salgınlarının yönetilmesi konusunda etkili olmuştur, bu kitlerin kullanımı konusu tablo7’ de ele alınmaktadır.
GENEL KANILAR
Aşı dışında bireysel bazda yapılması gereken bakım
Geçmişte aşılar her sene yapılmaktaydı. Yıllık aşı ziyaretleri, veterinerlerin olası bir hastalığı erken teşhis ve tedavisini sağlıyordu. Bunun yanısıra, yıllık ziyaretler hayvan sahiplerine kedi ve köpek sağlığının önemli noktaları üzerinde de bilgi vermeyi sağlıyordu.
Bu nedenle, çoğu hayvan sahibi, aşıların yıllık ziyaretin en önemli sebebi olduğunu düşünmeye başladı. Öte yandan veterinerler de aşı sıklığındaki azalma, müşterilerinin yıllık ziyaretleri unutmalarına, dolayısıyla hayvanın bakım kalitesinin düşnesine neden olacağından korktular. Bu nedenle veterinerler, her hayvan için bireysel bir sağlık programının önemi üzerinde durmalıdırlar. Bu programda, hayvanın ayrıntılı geçmişini, fiziksel kontrolünü, ve bireysel bakımını önceliklendirmelidir. Hayvan değerrlendirilirken, ağız sağlığı, düzgün beslenmesi, uygun testlerin yapılması, parazit kontrolü ve zoonotik hastalıklar kontrol edilmelidir. Davranışlarından bahsedilmelidir. Bunun yanısıra genç ve geriatrik hayvanlar, bazı hastalıklara meyilli özel ırklar özel bir kontrolle gözden geçirilmelidir. Aşı yıllık kontrolün sadece bir parçasıdır.
Düzenli( genellikle yıllık) kontrol sırasında, veteriner hayvanın temel ve temel olmayan aşılara gereksinimini değerlendirmelidir. Veteriner, müşteriye mevcut aşıları, bunların risk ve faydalarını, her hayvanın yaşam tarzı ve altında olduğu riskleri değerlendirerek anlatmalıdır. Çoğu temel aşı yıllık uygulama gerektirmezken, temel olmayan aşıları genellikle her yıl tekrarlamak gerektiğinden, bu yıllık kontroller sırasında hayvan aşılanacaktır. O bölgedeki yerel riskler de bu kontroller sırasında ele alınmalıdır. Riskleri azaltıcı öneriler de sunulmalıdır( kalabalıktan uzak durma, beslenmeyi iyileştirme ve enfeksiyonlu hayvanlarla aynı ortamda bulunmama gibi).
Aşılar, koruyucu sağlık planlamasının sadece bir parçasıdır. Bunun yanısıra, hayvanın yaşı, ırkı, sağlık durumu, yaşadığı çevre( zararlı etkenlere açık olma riski) , yaşam tarzı( diğer hayvanlarla kontağı) ve seyahat alışkanlığı da değerlendirilmelidir.
Hayvanın yaşı, koruyucu sağlık programında etkili bir elemandır. Yavru kedi ve köpeklere uygulanan programlar genellikle aşı, parazit kontrol ve kısırlaştırmayı içerir. Günümüzde, hayvan davranışı danışmaya yönelik ve hayvanlardan insanlara geçen hastalıkları önlemeye yönelik sağlık programları bulunmaktadır. Yaşlanan hayvan için, yaşlı hayvan bakım programları giderek populer hale gelmektedir. Beslenme, diş hastalıkları, parazit kontrol ve danışmanlık her hayvan için hayatı boyunca yapılması gereken değerlendirmelerdir. Yavruyken tam bir şekilde aşılanmış yetişkin kedi ve köpeklerin, özel bir temel aşı programına ihtiyaçları yoktur. (Day 2010, Horzinek 2010, Schultz ve diğerleri 2010). Araştırmalar göstermektedir ki, yaşlı kedi ve köpeklerin temel aşılarla devam eden bir bağışıklık hafızası bulunmaktadır: serumdaki antikor ölçümü bir sonuç vermektedir ve sadece bir doz aşıyla bu seviye arttırılabilmektedir (Day 2010) [EB1]. Yetişkin hayvanlarda temel aşının yeniden yapılması kararı, serolojik test sonucuna göre belirlenebilir. Veterinerlerin bu yöntemi önermesi, aşı sıklığı konusunda endişeleri olan hayvan sahipleri arasında olumlu karşılanmaktadır. Buna karşın yaşlı hayvanların, yeni antikorlara karşı etkin bir bağışıklık geliştirmesi zor olabilir. İngiltere’de, seyahat için ilk defa kuduz aşısı yapılan yaşlı köpeklerin yasal olarak istenen titre seviyesine ulaşmadığı görülmüştür (Kennedy ve diğerleri 2007) [EB1]. (15)
Evcil hayvanın içinde bulunduğu çevrenin sağlık durumunu yüksek seviyede etkilediği ve yıllık kontrolleri sırasında çevresindeki risk faktörlerinin mutlaka ele alınması ve bunlara karşı önlemler geliştirilmesi gerekliliği bilinmektedir.
Kedi ve köpeklerin, diğer hayvanlarla takip edilemeyen bir şekilde kontakt halinde bulunması, temel olmayan aşıların gerekliliğini belirler. Örneğin köpekler, hayvan pansiyonlarında kalabilir, kuaför salonlarına gidebilir veya diğer hayvanlarla ortak kullanılan yerlere, kenelerin bulunduğu alanlara veya başka enfeksiyonların bulaşma riski olan alanlara gidebilirler. Bu yerleri ziyaret sıklığı yapılacak aşıları değerlendirmede etkilidir.
Nasıl insanlar daha fazla seyahat ediyorsa, evcil hayvanlarda artık daha mobil hale gelmişlerdir. bu durumda enfeksiyonlar, parazitler, çevresel tehlikelerden kaynaklı çeşitli riskler sözkonusu olmaktadır. Veteriner kontrolleri sırasında geçmişte yaptığı ve gelecekte yapacağı seyahatleri gözönünde bulundurmak, yapılan koruyucu hizmetin bireyselleşmesine ve buna bağlı gerekli teşhisin yapılmasına yardımcı olacaktır.
Aşıyla İlgili Kayıtlar
Aşı uygulanırken, aşağıdaki bilgiler de kayıt altına alınmalıdır:
– aşının yapıldığı tarih
– aşıyı yapan kişinin kimliği,
– aşı adı, lot veya seri numarası, son kullanma tarihi ve üreticisi
– aşının yapıldığı yer ve uygulama şekli
Yapışkanlı aşı etiketleri ve medikal kayıt için mühür kullanılması, bazı ülkelerde zorunlu olan belgeleme işlemini kolaylaştırır. Görülen yan etkiler de , bir sonraki ziyarette diğer çalışanların göreceği şekilde not edilmelidir. Offlabel( yani prospektüste tavsiye edilen dışındaki kullanım) ilaç kullanımında, müşterinin bilgilendirildiğine ve bu uygulamaya izin verdiğine dair onaylı yazılı belge alınmalıdır. Bu belgede ayrıca, bu uygulamanın tüm risk ve faydalarının müşteriye anlatıldığı da belirtilmelidir.
VGG aşı belgelerinde, sadece aşının yapıldığı tarih değil, aynı zamanda bir sonraki aşının yapılması gereken tarihinin de işlenmesini önermektedir. Bu durum hayvan sahiplerinin ve pansiyon işletmecilerinin kafalarının karışmasına engel olacaktır.
Yan Etkiler
Yan etkiler, aşının uygulanmasıyla ilgili oluşan istenmeyen sonuçlar olarak tanımlanabilir( korumanın oluşmaması da dahil olmak üzere). Aşının yapılmasıyla birlikte hayvanda oluşan, aşıyla doğrudan bağlantılı olduğu gösterilemese de, herhangi bir yaralanma, zehirlenme veya duyarlılık reaksiyonudur. Yan etkiler, aşıyla ilgileri kanıtlandığı veya sadece süphelenildiği durumlarda bile raporlanmalıdır. Bu raporda, kullanılan ilaç, etkilenen hayvan ve raporu hazırlayan kişinin ismi belirtilmelidir.
Aşının uygulanması sırasında oluşan beklenmedik etkilerin raporlanması, üreticinin ve düzenleyici kurumun, ilacın olası etkinlik ve güvenlik problemlerini araştırması için bir imkan doğurduğu için önemlidir. Ruhsat almadan önce yapılan güvenlik araştırmalarının amacı, sık rastlanan yan etkilerin saptanmasıdır. Nadir yan etkiler ancak ilaç piyasaya sürüldükten sonra, raporlanan yan etkilerin incelenmesiyle ortaya çıkacaktır. Birçok ülkede devlet kurumları bu konuyu incelemez, bu nedenle oluşan reaksiyonların üretici firmaya iletilmesi gerekmektedir. VGG, bu konuda yapılan araştırmalara dayanarak, aşıların yan etkilerini çok az düzeyde raporlandığına inanmaktadır [EB4]. Bu nedenle tüm veterinerlere gerekli raporlamayı yapmalarını önermektedir.
Eğer herhangi bir yan etki iyi bir şekilde belgelenirse, hazırlanan rapor, bu konudaki yazılacak diğer raporlarla bir karşılaştırma sağlaması açısından önem taşımaktadır. Ayrıca raporlanan yan etkiler, daha önce farkına varılmamış reaksiyonların belirlenmesine, belirlenen reaksiyonların aslında daha fazla olduğunun gösterilmesine, reaksiyonlara bağlı risk faktörlerinin belirlenmesine ve bu yolla daha fazla klinik, epidemiolojik ve laboratuvar araştırmalarının yapılmasına yol açar. Bu nedenle veterinerler, aşı uygulaması sırasında veya sonrasında meydana gelen anlamlı tüm yan etkileri raporlamalıdırlar. Bu şekilde bir raporlama, ilaca karşı bir suçlama değildir. Ürünün zaman içinde gözden geçirilmesini ve daha güvenilir hale gelmesini sağlayan bir yoldur.
EKLER
EK 1- KEDİ VE KÖPEK ENFEKSİYONLARIYLA İLGİLİ BİLGİ NOTLARI
Bilgi Notu: CANINE PARVOVIRUS TİP 2 (CPV-2)
Mevcut Aşı Çeşitleri
Değiştirilmiş canlı aşılar( MLV): CPV-2 nin üç değişik türü bulunmaktadır: CPV-2a, CPV-2b ve CPV-2c’ dir. Günümüzde, aşı terkibinden çıkarılabilme imkanına rağmen, orjinal CPV-2 varyantı nadiren izole edilmektedir. En yeni varyant CPV-2c’ dir. Kuzey ve Güney Amerika, Avrupa, Afrika ve Asya’ da en bilinen genotiptir( genetik bileşendir) (Ohneiser ve diğerleri 2015). Bütün genetik bileşenler antijenler aracılığıyla birbirleriyle ilişki halindedir.Yapılan araştırmalar, CPV-2a ve CPV-2b bulunan aşılar köpeklere uygulandığında, CPV-2c de dahil olmak üzere tüm varyantlara karşı koruyucu bağışıklık sağladığı görülmüştür (Spibey ve diğerleri 2008, Decaro & Buonavoglia 2012, Wilson ve diğerleri 2013). Bir araştırmada bunun tersini gösteren bir durum görülmüştür (Decaro ve diğerleri 2008). Bu köpekler, 42 günlükken, 57 günlükken ve 90 günlükken aşılanmış, yetişkin köpeklere de yıllık tekrar (booster) aşıları yapılmıştır.
İnaktif, cansız aşılar: az sayıda cansız CPV-2 aşısı bulunmaktadır. MLV aşılarıyla karşılaştırıldığında, daha az etkili ve daha geç bağışıklık cevabı oluştururlar (Pollock & Carmichael 1982b). Rutin kullanım için tavsiye edilmemektedirler. Cansız aşılar, az bulunan ve vahşi canlı türlerinde, bazı canlı aşı türlerinin tavsiye edilmediği hamile hayvanlarda kullanılabilir. Buna karşın, cansız CPV-2 aşılarının bu durumlarda etkili ve güvenli olduğu test edilmemiştir.
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- Köpeklerde doğal yollarla geçen enfeksiyondan, hastalıktan sonra oluşan bağışıklığın çoğunlukla hayat boyu olduğu düşünülmektedir,
- Canlı virüs içeren aşılarla yapılan aşıların oluşturduğu bağışıklığın, yapılan araştırma ve testlerin sonuçlarına göre en az 9 sene olduğu bilinmektedir (Schultz ve diğerleri 2010).
- Cansız viruslerle yapılan aşının bağışıklık süresi en az 3 senedir.
- Anneden yavruya geçen antikorların (MDA) oluşturduğu aktif bağışıklık yavruda, kolostrumda bulunan antikorlardaki titreye, doğumdan sonra absorbe edilen antikorların miktarına ve spesifik aşıya bağlı olarak değişiklik gösterir (Pollock & Carmichael 1982a).
- Hassas dönem (window of susceptibility) bir yavruda, aşının bağışıklık sağlamadığı fakat virusün enfekte ettiği dönem demektir. Etkili canlı virüslü (MLV) aşılarda(yüksek titreli, düşük geçişli) bu süre 2 haftayı bulur. Daha az etkili olan MLV aşılarda ise bu süre 10-12 hafta kadardır (Schultz & Larson, 1996, Hoare ve diğerleri1997).
- Yavrulara yapılan aşı serilerini 16 haftalıkken veya sonrasında tamamladıktan ve tekrar aşılarını 26. haftada veya 52. haftada yaptıktan sonra, 3 yıl boyunca yeniden aşı gerekmez.
- MDA’nın yetersiz olduğu durumlarda, MLV aşıları aşı yapıldıktan 3 gün sonra koruma sağlamaya başlar (Schultz&Larson,1996).
- Titreden bağımsız olarak serumda antikorların bulunması, aktif bir şekilde bağışıklık oluşmuş 20 haftadan büyük bir köpekte oluşan korumayla doğru orantılıdır.
Önlem alınması gereken durumlar
- MLV aşılar vahşi hayvanlarda kullanılmamalıdır.
- MLV aşılar hamile hayvanlarda aksi belirtilmedikçe kullanılmamalıdır
- 4 ila 6 haftadan küçük yavru köpekler MLV ürünlerle aşılanmamalıdır
Hastalığın seyri
- Enjeksiyondan sonra, hastalık belirtileri 3 ila 7 gün içinde kaybolur.
- 2 haftadan sonra dışkıda CPV-2 nadiren görülür.
- 4 haftadan daha uzun süren enfeksiyon belirlenmemiştir. Böyle bir durumda köpeğin ölmesi ya da bu süre zarfında virusten tamamen temizlenmiş olması beklenir.
- Virus bulunduğu ortamda en az bir yıl boyunca yaşayabilir. Bu nedenle enfeksiyonlu hayvanların bulunduğu tüm ortamlar da enfekte olmuş kabul edilmelidir.
- Bir yavrunun dışkısında tespit edilen pozitif antijenin ve hayvanda canine parvorial enteritis klinik belirtilerinin görülmesinin sebebinin yakınlarda yapılan bir CPV aşısı olmadığını araştırma sonucu göstermiştir(DeCaro ve diğerleri 2014).
BİLGİ NOTU: CANINE ADENOVIRUS (CAV)-2 AŞISI
CAV-2 aşıları ve mevcut aşı tipleri
MLV aşılar: İçinde CAV-2 bulunan aşılar en kolay bulunabilen aşılardandır. CAV-1 yüzünden oluşan Infectious Canine Hepatitis (ICH)e karşı koruma sağlayan tek aşıdır. Aynı zamanda CAV-2 enfeksiyonunun yol açtığı solunum yolları hastalığı belirtilerini yok eder. Bu aşılar çok etkindirler ve CAV-1 aşılarının yol açtığı alerjik uveitis ya da mavi göz hastalığı gibi yan etkileri göstermezler (Curtis & Barnett, 1983). Parenteral yolla uygulanan CAV-2 canlı aşılarının yanısıra, canine infectious respiratory disease complex, bordetalla bronchiseptica ve canine parainfluenza viruslerini ( cpiv) barındırır. Burun içi uygulanan ürün CAV-2 ve CPIV ve Bordetalla ihtiva eder ve CIRDC’nin şiddetli seyretmesine engel olur. Fakat, ICH’ yi engelleyici tek aşı olarak kullanılmamalıdır. Bu nedenle, parenteral yoldan canlı CAV-2 aşısı da uygulanmalıdır.
İnaktive edilimiş( cansız) aşılar: cansız CAV-1 ve CAV-2 aşıları bazı ülkelerde kullanılmaktadır, ancak MLV yani canlı aşıların bulunduğu durumlarda tavsiye edilmemektedir. Çünkü daha az etkilidirler.
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- Doğal yollardan bulaşan hepatit enfeksiyonunda, koruma köpeklerin büyük çoğunluğunda hayat boyu devam eder,
- Canlı virüs içeren aşılarla yapılan aşıların oluşturduğu bağışıklığın, yapılan araştırma ve testlerin sonuçlarına göre en az 9 sene olduğu bilinmektedir(Schultz ve diğerleri 2010).
- Cansız CAV1 ve CAV2 virusleriyle yapılan aşının bağışıklık süresi canlı aşılardan daha kısadır.
- Anneden geçen antikorlar, parenteral yolla yapılan aşının tutmasına engel olabilir, bu nedenle yavru köpek son doz 16 haftalıkken diğer temel aşılarla birlikte yapılmalıdır.
- Yavrulara yapılan aşı serilerini 16 hafta ve sonrasında tamamladıktan ve tekrar aşılarını 26. haftada veya 52. haftada yaptıktan sonra, 3 yıl boyunca yeniden aşı gerekmez.
- MDA’nın bulunmadığı durumlarda, canlı aşılar ICH’ye karşı en erken 5 gün sonra koruma oluşturmaya başlar.
- Serumdaki antikorların bulunması, titreden bağımsız olarak, aktif bir şekilde bağışıklık oluşmuş 20 haftadan büyük bir köpekte korumayla doğru orantılıdır.
Önlemler
Burun yoluyla yapılan CAV-2 aşısı üst solunum yolları enfeksiyonunu engelleme amaçlı bir ek yöntemdir ve CAV-1 enfeksiyonuna karşı korumaz.
Hastalığın seyri
- CAV-1 ve CAV-2 birincil olarak tükürük ve idrar gibi vücut salgılarıyla bulaşır
- CAV-1 ve CAV-2 , bulundukları ortamda birkaç günden birkaç haftaya kadar yaşayabilirler
- Yapılan deneyde, CAV-1’ le enfekte olan bir hayvanda ICH belirtilerinin 5 günden sonrada ortaya çıktığı görülmüştür.
- Hassas dönem ( windows of susceptibility) bir yavruda, aşının bağışıklık sağlamadığı fakat virusün enfekte ettiği dönem demektir. CPV-2 aşılarının tersine uzun bir şüphe dönemi bulunmamaktadır( 2 haftadan kısadır).
- CAV-2 solunum yoluyla bulaşır.
- CIRDC hastalığının seyri farklıdır. Stres, yetersiz havalandırma, toz, tuvaletlerdeki amonyak gazı ve streptococcus, bordetella bronchisepica ve mycoplasma spp. gibi enfeksiyonlar, CAV2, CPIV, CIV, canine pneumovirus ve solunum yolları coronavirus etken olabilir
- CAV-2, CIRDC ile bir araya gelip 3-4 gün içinde solunum yolları enfeksiyonu oluşturur.
- CIRDC’nin oluşmasında çok farklı etkenler vardır ve aşıyla önlenemez. Mevcut aşılar sadece hastalığın şiddetini azaltmada etkilidir,
Bilgi Notu: Canine distemper virus (CDV)
Mevcut aşılar
MLV. En çok kullanılan ilaçlardır. Genellikle, farklı titrelerdeki Rockborn, Snyder Hill, Onderstepoort, Lederle CDV türlerini-suşlarını bulundururlar. CDV’ nin birçok tipi bulunmaktadır (Kapil ve diğerleri 2008, Espinal ve diğerleri 2014) ve bunlar farklı klinik belirtiler gösterir. Bu farklı türler arasında serolojik fark oldukça azdır. Mevcut aşılardan herhangi birinin uygulanması, bu farklı türlere karşı koruma oluşturacaktır. MLV aşılar vahşi hayvan türleri üzerinde aksini gösteren bir kanıt olmadığı sürece kesinlikle uygulanmamalıdır.
Vector Recombinant (rCDV) aşılar. ABD’ de Canarypox rekombinanı olan bir ürün bulunmaktadır . Özel bir canarypox vektör rekombinanı içeren ilaçlar vahsi hayvanlarda ve ekzotik türlerde de kullanılmaktadır (Connolly ve diğerleri 2013).
Cansız aşılar. Bu aşılar hazır bir şekilde bulunmazlar, etkili değildirler ve bu yüzden hastalığa karşı bağışıklık kazanmada kullanılmaması gerekir. Bazı vahşi hayvan türleri hariç.
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- Doğal yollardan bulaşan enfeksiyonda, koruma köpeklerin büyük çoğunluğunda hayat boyu devam eder.
- Canlı virüs içeren aşılarla yapılan aşıların oluşturduğu bağışıklığın, yapılan araştırma ve testlerin sonuçlarına göre en az 9 sene olduğu bilinmektedir(Schultz ve diğerleri 2010).
- rCDV aşısı uygulandıktan sonra koruma süresi challenge test’e göre en az 5 yıl, kan testine göre en az 6 yıldır.
- Cansız aşı uygulandıktan sonra koruma sütesi, MLV veya rekombinan aşılara göre daha kısadır.
- Anneden geçen antikorlar, parenteral yolla yapılan aşının tutmasına engel olabilir, bu nedenle yavru köpek 16 haftalıkken son doz diğer temel aşılarla birlikte yapılmalıdır.
- Hassas dönem (window of susceptibility) bir yavruda, aşının bağışıklık sağlamadığı fakat virusün enfekte ettiği dönem demektir. CPV-2’nin tersine, CDV aşılarında uzun bir hassas dönem bulunmamaktadır (2 haftadan kısadır).
- Yavrulara yapılan MLV aşılara, ruhsatında özel bir ibare bulunmadığı durumlarda 6 haftalıktan önce başlanmamalıdır (bazı ürünler 4 haftalıkken de kullanılabilir). Yavrulara yapılan aşı serilerini 16 hafta ve sonrasında tamamladıktan ve tekrar aşılarını 26. haftada veya 52. haftada yaptıktan sonra, 3 yıl boyunca yeniden aşı gerekmez.
- MDA’nın bulunmadığı durumlarda, canlı ve rekombinan aşılar çabuk bir şekilde koruma oluşturmaya başlar.
- Serumdaki antikorların bulunması, titreden bağımsız olarak, aktif bir şekilde bağışıklık oluşmuş 20 haftadan büyük bir köpekte korumayla doğru orantılıdır.
Önlemler
- Canlı aşılar evcil köpeklere uygulanabilir. Vahşi ve egzotik hayvanlara yapılması güvenli değildir. Bu aşılar yüksek derecede virulandır ve vahşi hayvanlarda(örn. Siyah ayaklı gelincik ve gri tilkide) hastalık ve ölüme sebep olur (Carpenter ve diğerleri 1976, Pearson 1977, Durchfeld ve diğerleri 1990). Ürünün bu türlere uygulanmasının güvenli olduğunu destekleyecek bilgi bulunmadığı sürece, bu türlere aşı uygulanmamalıdır.
- 4-6 haftalıktan küçük köpeklere MLV aşılar uygulanmamalıdır.
Hastalık seyri
- Enfeksiyon bulaştıktan sonra 2 ila 6 hafta içinde görülür.
- Kuluçka devrinde CDV kendini bağışıklıkta zayıflama( immunosüpresyon) olarak gösterir. Bu da hayvanı mikrobik hastalıklara karşı zayıf hale getirir. Gençlik hastalığı virüsüne bağlı belirtiler oluşmadan ikincil olarak gelişen hastalıklar, solunum yolları hastalıklarına, pneumoni ve ölüme sebep olabilir
- Ortamdaki virüs kısa sürede etkisini kaybeder.
BİLGİ NOTU: FELİNE PARVOVİRUS AŞILARI (FPV)
Mevcut Aşı Çeşitleri
Canlı aşılar(MLV): Bu aşılar adjuvansız fzrklı titrelerde avirulan feline parvovirus (feline panleukopenia virus) içerir. Enjekte edilen veya burun yoluyla uygulanan ve FCV, FHV-1 de içeren karışımlar bulunmaktadır. Canlı aşılar daha hızlı etki ederler. Anneden geçen antikorlar üzerinde daha etkilidirler ve yeterli derecede bağışıklık oluşturma olasılıkları daha yüksektir (DiGangi ve diğerleri 2011, Lappin 2012) Burun yoluyla yapılan FPV karışımları barınaklarda uygulanmamalıdır; FCV/FHV-1’ e karşı uygulanacaksa da aynı zamanda parenteral yolla canlı FPV aşısı da yapılmalıdır (Schultz, 2009).
Cansız aşılar: cansız adjuvanlı FPV aşıları bulunmaktadır, enjekte edilen bir doz aşı kısa bir sürede iyi bir bağışıklık oluşturur. Öte yandan, tüm cansız FPV aşıların, 2 ila 4 hafta arasında tekrarlanması gerekir. Bağışıklık 2. uygulamadan sonra oluşur. Cansız aşılar ekzotik veya vahsi hayvan türleri, hamile hayvanlarda, retroviral enfeksiyonu olan hayvanlar üzerinde etkili olabilir
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- Enfeksiyon veya hastalıktan sonraki koruma süresi ömür boyudur.
- Canlı aşı uygulamadan sonra, challenge ve serolojik testlerin gösterdiği koruma süresi en az 7 senedir.
- Cansız panleukopenia ile yapılan aşının ardından oluşan bağışıklık süresinin en az 7.5 yıl olduğu görülmüştür(Scott & Geissinger1999).
- Feline panleukopenia görülen birçok vakada buna FPV enfeksiyonun neden olduğu görülmüştür. Kedileri enfekte eden ve hasta olmalarına sebep olan Canine parvovirus’ün varyantları (CPV-2a, CPV-2b ve CPV-2c) ortaya çıkmıştır (Decaro & Buonavoglia 2012). Bazı FPV aşıları bu CPV varyantlarına karşı koruma oluşturmaktadır.
- Yavru kedide varolan anneden yavruya geçen antikorların oluşturuğu aktif bağışıklık yavruda , kolostral antikorlardaki titreye, doğumdan sonra absorbe edilen antikorların miktarına ve spesifik aşıya bağlı olarak değişiklik gösterir.
- Hassas dönem bir yavruda, aşının bağışıklık sağlamadığı fakat virusün enfekte ettiği döneme denmektedir, canine parvovirus’de olduğu gibi, antikor seviyelerinin doğal yolla geçen hastalığa karşı korumak için düşük olduğu, ancak aşının tutmasını engelleyecek kadar çok olduğu bu dönemde bir bağışıklık boşluğu oluşur.
- Yavrulara yapılan aşı serilerini 16 hafta civarı tamamladıktwn ve tekrar aşılarını 26. Haftada veya 52. Haftada yaptıktan sonra, 3 yıl boyunca yeniden aşı gerekmez.
- Serumdaki antikorların bulunması, titreden bağımsız olarak, aktif bir şekilde bağışıklık oluşmuş 20 haftadan büyük bir köpekte korumayla doğru orantılıdır.
- Eğer barınakta bir salgının önüne geçilmek isteniyorsa. Mlv aşıların kullanılmasnın çabuk bir şekilde bağışıklık oluşturmak gibi abantajları vardır.
- Canlı viruslü aşılar, aşıdan sonra çok kısa sürede bağışıklık oluşturur (Brun & Chappuis 1979).
Önlemler
- MLV FPV aşılar, tersi ispatlanmadığı takdirde vahşi hayvanlar üzerinde kullanılmamalıdır.
- MLV FPV aşılar hamile hayvanlarda kullanılmamalıdır. Çünkü virüsün fetusa geçmesi ve zarar vermesi mümkündür. Bazı ülkelerde hamile hayvanlara cansız virüslü aşılar yapılmaktadır. Ancak hamile hayvanlara gereksiz uygulamalrdan kaçınılmalıdır.
- MLV FPV aşılar 4 ila 6 haftadan küçük kedilere uygulanmamalıdır. Beyincikleri gelişme sürecinde olduğu için xarar görebilir.
- Bağışıklığı baskılanmış( immunosuppressed) hayvanlarda MLV FPV aşılar kullanılmamalıdır. Risk fazla olmasa da , ciddi immunosupresyon durumlarında, örneğin FIV veya FeLV sözkonusuysa, veya immunosupresif ilaçlar kullanılımı sözkonusuysa, aşıdan sonra hastalık belirtileri görülebilir.
Hastalık seyri
- Enfeksiyondan sonra hastalık belirtileri 2 ila 7 gün arasında kaybolur.
- Ateşi izleyen 1-2 günde kusma görülür. İshal daha sonra olur ama her zaman görülmez. Hayvanda dehidratasyon çabuk gelişir. Hasta bir kedi su kabının başında susamış bir vaziyette oturur, ancak içmez. Son aşamalarında hipotermi görülür. Septik şok oluşur ve damariçi pıhtılaşma görülür.
- Virus en az 1 yıl boyunca yaşamını sürdürür (Gordon & Angrick 1986). Bu nedenle enfekte hayvanların bulunduğu tüm alanlar kontamine kabul edilmelidir.
BİLGİ NOTU: FELİNE HERPES VİRUS (FHV-1) Aşısı
MLV aşı: Bu aşılar, adjuvansız, farklı titrelerde attenue FHV1(feline rhinotracheitis virusu tek bir serogrup oluştur) içerir. Enjekte edilebilen ve burun yoluyla uygulanan tek bir antijen içeren veya başka antijenler içeren karışımlar bulunmaktadır( her zaman FCV bulunmaktadır)
Cansız aşılar: adjuvanlı cansız aşılar piyasada mevcuttur.
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- FHV1 aşıları (FCV aşıları da ) FPV aşılarının olduğu gibi tam koruma sağlamazlar. Kedilere uygulanan diğer iki temel aşı( FHV1 ve FCV) FPV’ ninki ya da köpeklerin temel aşıları kadar güçlü koruma sağlamazlar ve koruma süreleri onlara benzemez
- Koruma sürelerini değerlendirmek zordur. Koruma aşıdan hemen sonra oluşur ve zaman içinde koruma süresi azalır (Gaskell ve diğerleri, 2007)
- Bağışıklık farklı sürelerde korur ve enfeksiyonve hastalıktan sonra çok sağlam olmaz
- Cansız bir FHV-1 aşısıyla yapılan aşının ardından antikor titresi 3 yıl boyunca dayanıklılık göstermiştir, ancak antikor titresi korumayla korele değildir (Scott & Geissinger 1997)
- 2 doz cansız virulan FHV-1 aşısı ile yapılan aşının sağladığı koruma, 7,5 yıl sonra tam değildir, cansız aşının 1 yıl sonra sağladığı korumaya benzer. (Scott & Geissinger 1999).
- Yavrulara yapılan aşı serilerini 16 hafta civarı tamamladıktan ve tekrar aşılarını 26. Haftada veya 52. Haftada yaptıktan sonra, düşük riskli kedilerde 3 yıl boyunca yeniden aşı gerekmez. Fakat yüksek risk altındaki kediler( mesela sık sık hayvan pansiyonlarında kalan kediler) daha sık aşılanmalıdır.
- Eğer tekrar aşısında bir gecikme olursa, daha önceki aşıları tam olan bir kediye yapılacak bir doz aşı, bağışıklık hafızasını yükseltmeye yeterlidir.
- Virulan bir viruse karşı hiçbir herpes virus aşısı koruma sağlamaz; FHV1 gizli kalıp şiddetli stres dönemlerinde ortaya çıkabilir. Reaktive olmuş virus, aşılı hayvanlarda da klinik belirtiler gösterir (Gaskell ve diğerleri 2007). Virüs zayıf hayvanlara geçip onlarda da hastalık oluşturabilirler (Gaskell ve diğerleri 2007).
- Hücrenin aracılık ettiği bağışıklık(cell mediated immunity), korumada önemli bir rol oynamaktadır. Aşılı kedilerde serumda antikor bulunmaması, bu kedilerin hastalığa açık olduğunu göstermez.
- Yavru kedide varolan anneden yavruya geçen antikorların (MDA) oluşturduğu aktif bağışıklık yavruda , kolostrumdaki antikorlardaki titreye, doğumdan sonra absorbe edilen antikorların miktarına ve spesifik aşıya bağlı olarak değişiklik gösterir. İlk aşılara 6-8 hafta civarı başlanır. MDA genellikle burundan yapılan aşılarla parenteral yolla yapılan aşılara göre daha az etkileşim gösterir. MDA’lı kedilerde burun yoluyla yapılan aşılar parenteral yolla yapılan aşılara göre daha erken koruma sağlar.
- Kedi üretim merkezlerinde yavru kedilerde hastalık genellikle sütten kesilmeden önce, 4 ila 8. haftalarda MDA’nın azaldığı dönemde görülür. Çoğunlukla hastalık kaynağı annedir, gizli olan virus doğum ve emzirmenin getirdiği zayıflıkla aktive olur.
Önlemler
- Değiştirilmiş canlı FHV1 ve FCV aşıları parenteral yolla yanlış bir şekilde uygulandığında, bazı patojenik potansiyelleri olduğu için hastalığa sebep olabilirler(örneğin yanlışlıkla burna sıkıldığında veya kazayla ciltten tüyden emilip, yalandığında).
- Burun yoluyla yapılan aşıdan sonra kimi zaman üst solunum yolları enfeksiyonu görülmektedir.
Hastalık seyri
- Viral salgılama enfeksiyon başladıktan sonraki 24 saat içinde başlar ve 1 ila 3 hafta sürer.
- Akut hastalık 2-6 gün içinde görülür ve 10-14 gün sonra son bulur.
- Virus sinirler boyunca ilerleyip, nöronal hücrelere özellikle tregemimal ganglia’ya ulaşır ve gizlice yerleşir. Çoğu kedi yaşam boyu gizli taşıyıcı hale gelir. Virus ara ara ortaya çıkar. FCV nin yeniden ortaya çıkışı devamlı bir şekilde, enfeksiyonu izleyen aylarda olur (Gaskell ve diğerleri 2007). Herpes virüsünün genomik DNA’sı,enfekte olmuş nöronun nukleusunda , çoğalma olmadan yaşar.
- Virus bulunduğu ortamda kullanılacak dezenfektanlarla etkisiz hale gelir.
BİLGİ NOTU:FELİNE CALİCİVİRUS(FCV)AŞILARI
Mevcut Aşılar
Canlı aşılar: Adjuvansız f9 suşundan(türünden) feline calicivirus bulundururlar. Sade olarak bulunan veya diğer aşı antijenlerini ( her zaman feline herpes virus vardır)barındıran enjekte edilebilen veya burun yoluyla uygulanabilen karışımlardır.
Cansız aşılar: Adjuvanlı cansız aşılar da bulunmaktadır, adjuvansız bir cansız aşı 2 calicivirus suşu barındırmakdır( G1 ve 431 suşları, Poulet ve diğerleri 2005).
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- FCV türleri arasında antijen açısından farklılıklar vardır. Bir türle enfekte olmak, heterolog(kaynakları farklı) türlerle karşı karşıya kalındığında, akut klinik belirtileri ve virus bulaşımını azaltır. Heterolog korumanın derecesi genellikle incelenen virus suşlarına bağlıdır.
- Antikorları etkisiz hale getiren virus genellikle enfeksiyondan 7 gün sonra görülür; titreleri homolog( benzer kaynaklı) challenge testle korreledir. Serumda antikor bulunmadığı durumlarda kediler yine de korunabilirler. Aşılı kedilerde, lokal salgısal IgA antikoru ve hücresel cevapların koruma oluşturduğu görülmüştür.
- Adjuvanlı ve cansız FCV aşısı uygulandıktan sonra, antikorların en az 4 yıl varoldukları görülmüştür(Scott & Geissinger 1997).
- 2 doz cansız adjuvanlı FCV aşısıyla yapılan aşıdan 7.5 yıl sonra korumanın eksik olduğu görülmüştür. Ancak koruma cansız bir aşıyla yapılan aşıdan 1 yıl sonraki durum gibidir (Scott & Geissinger 1999).
- FCV tarafından sağlanan koruma( FHV1 tarafından da) FPV‘ninki kadar tam değildir. Bu iki temel aşının sağladığı korumanın ve koruma süresinin FPV veya köpek temel aşılarınınki kadar olması beklenmemelidir. Aşılı kedilerde, FCV enfeksiyonunun veya ülme olasılığı bulunmaktadır.
- Yavrulara yapılan aşı serilerini 16 hafta civarı tamamladıktwn ve tekrar aşılarını 26. Haftada veya 52. Haftada yaptıktan sonra, 3 yıl boyunca yeniden aşı gerekmez. Yüksek riskli kedilerin daha soık aşılanması gerekebilir.
- Yavrulara yapılan aşı serilerini 16 hafta civarı tamamladıktan ve tekrar aşılarını 26. Haftada veya 52. Haftada yaptıktan sonra,ö3 yıl boyunca yeniden aşı gerekmez. Yüksek riskli kedilerin daha sık aşılanması gerekebilir.
- Kedi yavrularına seri halde yapılan aşıalrda aynı suştaki aşılar uygulanmalıdır.
- Yavrularda ilk günlerinde MDA’nın varlığı önemlidir. MDA’nın ortalama yarı yaşam süresi 15 gündür, ancak 10 ila 14 haftaya kadar yaşamını sürdürür (Johnson & Povey 1983). Yapılan bir alan araştırmasında 6 haftalık yavru kedilerin %20’ sinde çokça kullanılan bir aşı suşu uygulamasına karşı hiç antikor bulunmamıştır (Dawson ve diğerleri 2001). MDA, burun yoluyla MLV aşı uygulamasında parenteral yolla MLV aşı uygulamasına göre daha az etkileşim halindedir. MDA’lı kedilerde burun yoluyla uygulamanın parenteral yolla uygulanan aşılara göre daha çabuk bağışıklık yarattığı görülmüştür.
Önlemler
- Bazı durumlarda, burun içi uygulamanın bir komplikasyonu olarak üst solunum yolları enfeksiyonu görülebilir.(Lappin ve diğerleri 2006, 2009).
- Antijen açısından farklı virüslerin varlığı, aşılardaki türlerin kombinasyonu şiddetli hastalıklara koruyacak şekilde geliştirilmiştir, hafif hastalıklar aşılı kedilerde de olabilir.
Hastalığın seyri
- FCV enfeksiyonu, akut şekilde oral ve üst solunum yolları enfeksiyonuna neden olabilir. Özellikle bağışıklıkla ilgili kronik gingivostomatitit ortaya çıkabilir.
- Kuluçka dönemi 2 ila 10 gündür. Ağızda oluşan ülserler( özellikle dilin yan tarafları) görülür, hayvanda görülen hapşırma ve ciddi burun akıntısı belirtilerdendir. Yavru kedilerde ağız hastalıkları ve üst solunum yollar hastalıkları görülür.
- Bazı durumlarda farklı bir sendrom olan virulant systemic calicivirus (VS-FCV) hastalığı görülür (Coyne ve diğerleri 2006b).Bu hastalığın kuluçka dönemi, barınak ve kliniklerdeki kedilerde 1 ila 5 gündür. Ev ortamında 12 günü bulur. Bu hastalık yetişkinlerde yavrulara göre daha şiddetli seyreder. Mevcut aşıların yapılması kedileri sahalardaki enfeksiyondan korumaz, ancak deneylerde biraz koruduğu görülmüştür (Poulet & Lemeter 2008, Huang ve diğerleri 2010). Bu hipervirulan suş özelliğine bağlıdır. ABD’deki aşıda cansız VS- FCV suşu bulunmaktadır. Bu aşı geleneksel izolatların (isolates) yanısıra VS-FCV izolatları da bulundurur. Yapılan araştırmalarda homolog VS-FCV’ye karşı koruma sağladığı belirtilmiştir (Huang ve diğerleri 2010). Bu suştaki VS-FCV’nin heterolog VS-FCV türünekarşı koruma sağlayıp sağlamadığı bilinmemektedir.
BİLGİ NOTU: KUDUZ AŞILARI
Mevcut Aşılar
Canlı (MLV) aşılar. Bu aşılar kedi ve köpeklerin yanısıra, vahsi hayvanların oral yolla bağışıklık kazanmasında da kullanılmaktadır.( örneğin Kanada ve Avrupa’ da tilkilerde, Finlandiya’da rakunlarda kullanılmaktadır). Hepsi Streer Alabama Dufferin(SAD) virusünden türemiş güvenli virus suşlarıdır.
Vectored rekombinant kuduz aşıları. Rekombinan aşılardaki virusler güvenlidir. Çünkü sadece kuduz virüsünün koruma sağlayan G glycoproteinini bulundururlar. Çiçek virüsü( poxvirus- vaccinia ve canarypox) ve adenovirus vektörleri kuduz virusünün glycoproteinini ifade ederler ve Kuzey Amerika’da rutin olarak vahşi yaşamda kuduzu kontrol etmek için kullanılırlar. Oral yolla kullanılırlar. Kedilerde (canarypox vector) parenteral yolla kullanılır. Bu aşılar kuşlarda ve memelilerde avirulandır.
İnaktif- cansız aşılar. Cansız aşıların bireysel bazda veya toplu olarak kedi ve köpekleri kuduzdan korumak için uygulanması genel olarak bir kuraldır. Cansız aşılar ortam sıcaklığında muhafaza etmek kolaydır ve yanlışlıkla kendine yapılan enjeksiyonlar, MLV aşılarda olduğu gibi bir risk teşkil etmez.
Bağışıklık Mekanizmasının Oluşması ve Bağışıklık Süresi
- Kedi ve köpeklerdeki kuduz büyük ölçüde cansız aşılarla kontrol edilir. Fakat ABD ve Avrupa’da kediler için recombinant canary pox virus vectored aşısı ruhsat almıştır ve kullanılır. Çünkü enjeksiyon yerinde adjuvanlı kuduz aşıları gibi bir enflamasyon oluşturmaz(Day ve diğerleri 2007). İlk yapılan aşıdan sonra ikinci aşı 1 yıl sonra yapılmalıdır. Ancak ondan sonra yapılacak aşılar, 3 yıllık koruma süresi olarak ruhsat almış ilaçlarla 3 yıl sonra yapılabilir.
- Doğal yolla oluşan enfeksiyonunun koruma süresi değerlendirilemektedir. Çünkü enfeksiyonu takip eden hastalık kedi ve köpeklerde ölümcüldür.
- Challenge ve serolojik testlere göre cansız ve rekombinan ticari ilaçlarla yapılan aşıdan sonra koruma süresi 3 senedir(Jas ve diğerleri 2012).
- İlk aşı hayvan 12 haftalık olmadan yapılmamalıdır. Tekrarı 1 sene sonra yapılır. Aşıdan 4 hafta sonra antikor seviyeleri genellikle koruma oluşturucu seviyeye ulaşır. Serolojik testin gerekli olduğu durumlarda, aşı ve testin yapılması arasında geçen süre önemlidir ve kullanılan ürüne bağlıdır. İlacın prospektüsü ve yasal zorunluluklar dikkate alınmalıdır.
- Bazı aşıların virulan kuduz virüsüne karşı 3 sene koruduğu ispatlanmış olsa da, ulusal ya da yerel düzenlemeler her sene aşı yapmayı zorunlu kılabilir. VGG tüm yasal düzenlemelerin bilimsel gelişmeleri gözönünde bulundurmasını önermektedir. Bazı ilaçlar da örneğin ulusal düzeyde üretilen 1 yıldan fazla güvenilir bir şekilde korumaz.
- 16 haftalıktan daha büyük bir köpekte, serumdaki antikor seviyesinin ≥0.5 IU/ml olması korumanın oluştuğunu gösterir.
- Uluslararası evcil hayvan seyahati yasal zorunluluklarına göre aşıdan sonra yapılan serolojik testte serumda antikor seviyesi 0.05 IU/ml’den büyük olmalıdır
Hastalığın Seyri
- Hastalık belirtileri enfeksiyondan sonra 2 hafta ila birkaç ay arasında kendini gösterir. Yaranın oluştuğu yere bağlıdır. Geçiş genellikle ısırık veya tırmalama ile olur. Açıklanamayan agresif davranış veya ani davranış değişikliği şüpheyle karşılanmalıdır.
- Hastalık kendini sinirli veya sessiz bir şekilde gösterebilir. Sinirli bir şekilde seyreden kuduz vakalarında, gözkapağı, kornea ve gözbebeği reflekslerinde azalma, strabismus, düşük çene, salya salgılama, pika, ani nöbetler, kaslarda seyirme ve istemsiz titremeler, şaşılık, yön kaybı, amaçsızca yürüme, amaçsız ısırma, aşırı duygusal cevaplar, photofobia(ışıktan rahatsız olma), ataksi ve felç görülür. En son nokta koma ve solunum durması sonucu ölümdür. Kuduzun sessiz formu köpekler arasında kedilere göre daha sık görülür. Alt motor nöron paralizi ısırılan noktadan yayılıp tüm merkezi sinir sistemini etkiler. Felç kısa sürede komaya ve solunum yetmezliğine götürür.
Ortamda virüs etkisini çabuk kaybeder. Deterjan bazlı dezenfektanlarla kısa sürede inaktive edilir.
EK-2: SIKÇA SORULAN SORULAR
1. MLV bir aşıyı vahşi veya egzotik bir hayvan türüne ya da aşının ruhsatında belirtilen hayvan türleri dışında başka bir türe yapabilir miyim?
Hayır, bu türlerde kullanılmasının güvenli olduğu kanıtlanmamışsa kesinlikle yapılmamalıdır. Hatta, aşı vahşi hayvanlara uygulanırsa, bunlardan çıkan virusler tekrar virulan hale gelip, değişik evrelerden geçip, aslında tedavi etmesi gereken hayvan türlerinde de hastalık oluşturabilirler.
CDV’ye karşı zayıf olan türlerde güvenli ve efektif bir aşı “canarypox virus vectored recombinant” CDV aşısıdır. Bu aşı gelincikler için tek değerli(monovalent) bir formda kullanılır veya köpekler için bir kombinasyonu kullanılır. Monovalan aşı CDV olabilecek birçok vahşi ve egzotik türde kullanılmaktadır. Ancak sadece bazı ülkelerde mevcuttur.
2. CDV’ye karşı yüksek riski bulunan bir yavru köpeğe insanlara yapılan kızamık aşısı yapabilir miyim?
Hayır. Yetersiz miktardaki virus nedeniyle, insanlara yapılan kızamık aşısı, hayvanlarda bağışıklık oluşturmaz, köpekler için yapılan kızamık aşıları bazen CDV ve başka viral bileşenlerle kombine edilmiştir. Bunlar CDV ‘ye göre daha erken bir dönemde geçici bir koruma sağlarlar. 16 haftalıkken veya sonrasında, yavru CDV aşısıyla aşılandığında kalıcı bir bağışıklık kazanır.
3. Anneden geçen antikorlara (MDA) sahip yavru köpekler CDV’ ye karşı daha erken bir yaşta aşılanabilirler mi?
Evet. Köpekler için olan heterotipik kızamık aşıları kullanıldığında yavrularda MLV- CDV aşılarına göre 4 hafta daha erken bağışıklık sağlar. Aynı şekilde, “canarypox vectored recombinant” CDV aşısı, bazı MLV aşılarına göre 4 hafta daha erken bağışıklık oluşturabilir. Bazı yüksek titreli MLV aşıları( örneğin aşı ampulünde daha fazla miktarda virus barındıran aşılar) daha erken dönemlerde, mdalı yavrularda koruma oluşturabilir.
4. Anneden geçen antikorların( MDA) MLV aşılar söz konusu olduğunda aktif bağışıklık oluşmasına engel olduğu biliniyor. Cansız aşılar da bağışıklığı engellerler mi?
Evet. MDA bazı cansız aşıların tutmasını engeller. Eğer cansız aşının 2 doz yapılması gerekiyorsa ( ki genellikle böyledir), ilk dozun MDA yüzünden tutmadığı durumlarda, ikinci doz bağışıklık oluşturmaz. Bu durumda, ikinci doz ( eğer tutarsa) ilk doz gibi kabul edilerek bir üçüncü doz yapılmalıdır.
Bu durum, MLV aşılar için geçerli değildir. MDA’ nın bulunmadığı durumlarda yapılacak bir doz MLV aşı bağışıklık için yeterlidir. Fakat genellikle, özellikle genç hayvanlar söz konusu olduğunda, 2 doz aşı önerilir. Çünkü MDA azaldığında ve aşının tutmasına engel olmayacak seviyeye geldiğinde en azından bir doz yapıldığından emin olunması gerekir. Bu nedenle yavru kedilere ve köpeklere son doz 16 haftalık olduklarında veya sonrasında yapılır.
5. Köpeklere uygulanan bazı temel MLV aşıların, son dozun 10. hafta civarı olmak üzere 2 doz uygulanması gerektiği söylenmektedir? Bu doğru mudur?
VGG bazı aşıları erken bitirmenin erken sosyalleşmeyi sağlamak için önerildiğini düşünmektedir. Yavruların sosyalleşmesi önemlidir. Ancak VGG bu durumun bağışıklık ve korumanın geçerliliği üzerindeki muhtemel olumsuz etkilerine karşı temkinli yaklaşmaktadır. Hiçbir temel aşı karışımının son dozu 10 haftalıkken yapıldığında kabul edilebilir bir oranda bağışıklık sağlamaz. VGG mümkün olan durumlarda son dozun, öncesinde yapılan doz sayısından bağımsız olarak 16. hafta veya sonrasında yapılmasını önermektedir. VGG köpek sahiplerine, aşıları tamam olmayan yavruların dış dünyayla olan ilişkilerini kontrollü bir şekilde yapmalarını, sadece tam aşılı ve sağlıklı köpeklerle bir arada bulunmalarına izin vermelerini tavsiye etmektedir.
6. Aynı hastalığa karşı kullanılan ve parenteral ya da intranazal (burun yoluyla uygulanan) aşılar var mıdır?
Evet. Özellikle CIRDC’ye karşı olan köpek aşılarıyla kedilerde üst solunum yolları enfeksiyonuna karşı olan FCV ve FHV-1 aşıları böyledir.
Uygulamada dikkat edilmesi gereken noktalar bulunmaktadır. Parenteral yolla uygulanması gereken ( örneğin deri altı) FCV ve FHV-1 bulunduran MLV aşılar burun yoluyla veya oral yolla uygulanırsa ciddi hastalıklara sebep olunabilir. Eğer cansız FCV ve FHV-1 aşıları burun veya ağız yoluyla uygulanırsa, bağışıklık olmaz, aksine ciddi yan etkiler oluşur. Eğer intranazal canlı CIRDC parenteral yolla uygulanırsa, öldürücü etkili bir reaksiyon oluşur. Hatta köpek ölebilir. parenteral cansız bordetella aşısı da burun yoluyla uygulanırsa tutmaz, aşırı duyarlılık oluşturur.
Farklı uygulaması olan bu iki aşının birlikte uygulanması veya farklı zamanlarda uygulanması mümkündür. Parenteral ve intranazal uygulamanın birlikte yapılması sadece bir yere yapılan aşı uygulamasından daha iyi bir bağışıklık oluşturur (Reagan ve diğerleri 2014, Ellis 2015). Mesela parenteral uygulama ciğerlerde bir koruma sağlarken ( özellikle bölgesel salgısal IgA ve CMI-hücresel bağışıklık), üst solunum yollarında bir koruma oluşturmaz. Öte yandan intranazal uygulama iyi bir salgısal immunoglobulin A (secretory IgA) ve hücresel bağışıklık ve spesifik olmayan bağışıklık (örn.tip1 interferon) oluştururken akciğerlerde bir bağışıklık oluşturmaz.
7. Temel aşılar kullanıldığında köpeklerde ciddi hastalıklara karşı bağışıklık ne kadar zaman sonra oluşur?
Bu, hayvana, aşıya ve hastalığa bağlı olarak değişir.
En hızlı bağışıklık MLV canlı aşıların ve “recombinant canarypox virus vectored” CDV aşılarının kullanıldığı durumlarda oluşur. Bağışıklık cevabı dakikalardan saatlere varan kısa bir süre içinde oluşur ve MDA seviyesinden ve bağışıklık zaafiyeti bulunmasından bağımsız olarak 1 gün içinde korumaya başlar.
Eğer etkin bir MLV aşı kullanıldıysa, CPV-2 ve FPV’ ye bağışıklık 3 ila 5 gün içinde oluşur. Buna karşın cansız CPV-2 ve FPV aşılarının bağışıklık oluşturup koruması için en az 2-3 hafta geçmesi gerekir.
Parenteral yoldan uygulanan CAV-2 aşısı CAV-1’ e karşı bağışıklığı 5 ila 7 günde oluşturur. Ancak burun yoluyla uygulamada, parenteral yolla uygulanan aşıyla aynı derecede bağışıklık en az 2 hafta sonra oluşur, hatta bazı köpeklerde hiç oluşmaz. Bu nedenle CAV-1’ e karşı parenteral yolla uygulanan CAV-2 aşısı önerilmektedir.
FCV ve FIV-1 aşıları söz konusu olduğunda bağışıklık oluşturma süresini belirlemek zordur,çünkü bazı hayvanlarda koruyucu bağışıklık oluşmaz. Oluştuğundaysa, bu genellikle 7-14 gün sonra gerçekleşir (Lappin 2012).
8. Olması gerektiği gibi temel aşı uygulanmış yavru veya yetişkin kedi ve köpeklerde aşı etkinliği nasıldır?
Olması gerektiği gibi aşı yapılmış (canlı veya rekombinan CDV, CPV-2 ve CAV-2) köpeklerde, hastalığa karşı koruma en az % 98 oranındadır. Enfeksiyona karşı koruma da benzer bir yüksek oranda gerçekleşir.
MLV türü FPV aşısı gerektiği gibi uygulanan kedilerde en az % 98 oranında hastalığa ve enfeksiyona karşı koruma meydana gelir. Buna karşın FCV ve FHV-1 aşıları, çok fazla kontamine olmuş bir ortamda( örn. barınaklar) hastalığa karşı korusa da enfeksiyona karşı korumazlar. Yüksek riskli ortamlarda korumanın % 60-70 oranında gerçekleştiği görülmektedir. Koruma diğer kedilerden izole bir şekilde evde yaşayan veya yine aşılı kedilerle bir arada yaşayan kedilerde çok daha fazladır ve uzundur, çünkü hastalık riski azdır.
9. Mevcut aşılarla koruyucu bağışıklık oluşturulmayan CDV ve CPV-2’ nin mutant formları( biotip veya variant) var mıdır?
Bildiğimiz kadarıyla yoktur. Mevcut tüm CDV ve CPV-2 aşıları, CDV ve CPV-2’ nin bilinen tüm türlerine karşı, yapılan testlerin veya saha araştırmalarının sonuçlarına göre, koruma sağlamaktadır. Ancak, İtalya’daki köpeklerde meydana gelen bir CPV-2c salgını ve MLV aşıların kullanıldığını gösteren bir rapor bulunmaktadır. Yine aynı grup aşılı yaşlı köpeklerde CPV-2c hastalığının geliştiğini gösteren bir rapor bulunmaktadır.(Decaro ve diğerleri 2009).
10. Mevcut CPV-2 aşıları yeni CPV-2c varyantına karşı koruma sağlamakta mıdır? Bu koruma ne kadar sürmektedir?
Evet. CPV-2 aşıları, bulundurdukları varyanttan bağımsız olarak, aktif bir bağışıklık oluştururlar. Bu bağışıklık, köpeklerde, tüm CPV2 varyantlarına karşı ( 2a, 2b, ve 2c) en azından 4 yıl süren uzun vadeli bir koruma sağlar.
11. Parvovirus aşıları( canine parvovirus-2 ve feline parvovirus [panleukopenial] ) oral yolla uygulanabilir mi?
Hayır. Capv-2 ve FPV aşıları oral yolla verildiğinde bağışıklık oluşturmazlar. Burun yoluyla verildiğinde bağışıklık oluştururlar, ancak en etkin şekil parenteral yolun uygulanmasıdır ( deri altı veya kasiçi)
12. Bazı CPV-2 aşıları, MDA’ lı yavru köpeklerde diğer türlere göre daha erken bağışıklık oluşturabilir mi?
Evet. Bazı CPV-2 aşılarında daha yüksek viral titreler (örn.aşı ampulünde daha fazla miktarda virus) ve/veya daha fazla bağışıklık oluşturan ayrıştırılmış parçalar (isolates)(varyanttan bağımsız olarak) bulunmaktadır. Bunlar standart CPV-2 aşılarına göre birkaç hafta daha erken koruma oluştururlar.
13. Leptospira ( bakterili aşı) aşısı kullanıldığında, bu üründe 2 serogrup mu bulunmalı yoksa 2’den fazla serogrup mu olmalıdır?
Yüksek riskli köpeklerde Leptospira aşısı kullanıldığında, o bölgedeki köpeklerde hastalık oluşturan tüm serogrupların kullanıldığı ürün tercih edilmelidir. Birçok ülkede köpek popülasyonundaki seroguplar bilinmemektedir. VGG bu bilgilerin toplanmasını salık vermektedir.
14. Leptospira aşıları uzun süreli bağışıklık sağlarlar mı? Temel viral aşılar gibi etkin midirler?
Hayır. Leptospira aşıları nispeten kısa bir süre koruma sağlarlar. Aynı şekilde, özellikle aşının 6 aydan daha eski bir tarihte yapıldığı durumlarda, bazı Leptospira ürünleri klinik hastalığı önler ancak enfeksiyona karşı korumaz ve bakteri bulaştırmaya engel olmaz . Aşıdan sonra antikorlar sadece birkaç ay varlıklarını korurlar, bağışıklık hafızası da oldukça kısa süreli oluşur ( 1 yıl).
15. Herhangi bir feline leukaemia virüsü bulunduran aşılar ( ör. Cansız adjuvanlı, subunit, recombinant) sadece 1 dozla koruma sağlar mı?
Hayır. Bütün feline leukaemia virüsü bulunduran aşılar en azından 2 doz olarak uygulanmalıdır. 8 haftalıktan itibaren yavrulara 2-4 hafta aralıklarla 2 doz yapılmalıdır. Bu başlangıç serisi tamamlandıktan sonra, bir dozluk tekrar aşısı yapılabilir. Eğer başlangıç dozları arasında 6 haftadan daha fazla bir aralık olursa, aralıklar 2-4 hafta olacak şekilde kediye yeniden 2 doz aşı yapılmalıdır.
16. Kediler, yavruyken FeLV aşısıyla aşılanmışlarsa ve tekrar aşıları da yapılmışsa, yeniden aşılanmaları gerekir mi?
Hayır. Tekrar aşıları 2-3 yılda bir yapılmalıdır. Adjuvanlı aşılarla her sene yapılan aşılar enjeksiyona bağlı sarkoma oluşma riskini arttırır.
17. Ülkemde FIV aşısı neden yok?
Aşıların bir ülkede olup olmaması, aşı üreticisinin isteğine ve o ülkedeki düzenleyici kurumun ruhsat vermek için ülke şartları ve hastalığın ülkedeki seyrine göre ilacı değerlendirmesine bağlıdır. Mevcut FIV aşıları, FIV’ in iki alt tipini ( A ve D) bulundurur. Başka alt tiplere karşı koruma sağladığı ileri sürülse de, virusler ülkeden ülkeye değişiklik gösterir. FIV aşısı yapılacak kedilerde, aşıdan önce serumdaki antikorlar test edilmeli, aşıdan sonra da mikroçip takılmalıdır.
18. FIV aşısı yapılmış bir kedide FIV enfeksiyonu görülebilir mi?
Evet. Aşı herhangi bir FIV enfeksiyonunu engellemez, FIV virusunun tüm alt tiplerini de gizli olarak taşıyabilir. Bu nedenle FIV aşısı yapılan kediler enfeksiyon geçirebilirler ve zayıf kedilere hastalık bulaştırabilirler.
19. Mevcut CIRDC aşıları, CIV’ in neden olduğu hastalığa karşı koruma sağlarlar mı?
Hayır. Özel bir tür yarış köpekleri( racing greyhonds)nin CIV virüsüyle enfekte olduğu görülmüştür. Bunlar bir sene içinde rutin olarak 3 veya daha fazla kez CIRDC aşısıyla aşılanmışlardır. CIV antijenlerle alakalı olarak köpeklerde görülen herhangi bir virüsle bağlantılı değildir. Ancak H3N8 Equine Influenza virusüyle bağlantılıdır. ABD’ de mevcut CIV aşısı risk altındaki köpeklere önerilmektedir, 2015’ te yeni ortaya çıkan H3N2 virüsü için ABD’de geliştirilen ilaç, şarta bağlı olarak ruhsat almıştır.
20. CIV’ e karşı koruyan bir aşı bulunmakta mıdır?
Evet. ABD’ de, H3N8 virüsüne karşı bir aşı geliştirilmiştir. Bu, adjuvanlı cansız bir aşıdır. Diğer cansız aşılar gibi 2-4 haftalık aralıklarla 2 doz olarak uygulanması gerekmektedir. Bu alanda çalışmalar devam etmektedir, ve önümüzdeki yıllarda, hem etkinlik hem de daha uzun bağışıklık süresi için gelişmeler beklenmektedir.
21. Kedi ve köpekler için virüs, bakteri, mantar veya parazitlerin neden olduğu enfeksiyonlar dışında kullanılan aşılar var mıdır?
Evet. Özel bazı tür yılan sokmasına karşı geliştirilmiş aşılar vardır. Ayrıca, köpeklerde oral melanoma tedavisinde kullanılan bazı aşılar vardır.
22. Holistik karışımlar( nosodes) hayvanlarda bağışıklık yaratmak için kullanılabilir mi?
Hayır. Bu karışımlar herhangi bir hastalığı engellemez. Bağışıklık yaratmaz çünkü bunlarda antijen bulunmaz.
23. VGG canine enteric coronavirüs aşısının kullanılması konusunda ne düşünüyor?
Bu aşının koruma sağladığına dair herhangi bir kanıt yoktur, bu nedenle kullanılmasını önermiyoruz. Aslında köpekler için bir patojendir. Bu virusun farklı türlerinin (suş- strain) yavru köpeklerde ciddi sistemik hastalıklara sebep olduğu belirlenmiştir. Ancak mevcut aşıların bunlara karşı koruma sağlayıp sağlamayacağı açık değildir. Yapılan bir testte coronavirus çıkması hastalığın sebebinin bu olduğunu göstermez.
24. Monovalan( tek değerlikli)bir aşı multivalan( çok değerlikli) bir aşıya göre daha mı iyidir?
Mümkün olan en az sayıda bileşenli aşılar WSAVA kılavuzuna daha uygundur. Çoklu bileşenli MLV aşıları( örn. CDV, cav-2 ve CPV-2) temel aşı uygulamaları için idealdir. Fakat, temel olmayan antijenler için sadece tekli aşı önerilir( örneğin Leptospira, CIRDC) bu aşılar sadece risk fayda analizi yapıldıktan sonra kullanılması fayda yaratacağı düşünülüyorsa kullanılabilir. Çoklu bileşenli Leptospira aşıların formullerinde kullanılan çoklu serogrupların kullanımı yapılan bilimsel deneylerle desteklenebiliyorsa, bu aşılar en yüksek korumayı sağlar.
25. Multivalan aşılardaki farklı antijenlerin kullanımı aşının etkinliğini olumsuz şekilde etkiler mi?
Hayır. Multivalan bir aşının ruhsat alabilmesi için, “challenge studies” le üreticinin her bileşenin koruyucu bağışıklık geliştirmeye faydası olduğunu ispatlaması gerekir.
26. Aşı geçmişi bilinmeyen yetişkin bir köpeğe tüm aşılar bir seferde yapılabilir mi?
Evet. Yetişkin bir köpek aynı anda verilen bir çok antijene cevap verebilecek bir yapıdadır. Ancak, ilacın prospektüsünde belirtilmiyorsa, farklı aşılar aynı şırıngaya konulup, birlikte uygulanmamalıdır. Farklı aşıların farklı anatomik bölgelere yapılması uygun olacaktır. Bu yolla farklı lenf sistemleri bağışıklık cevabı oluşturabilir. Ancak bu bilimsel olarak ispatlanmamıştır.
27. MLV aşılarla genetiği değiştirilmiş aşılar arasında ne fark vardır?
Genetiği değiştirilmiş aşılar, virus vectored aşıları, genetik olarak mutasyona uğramış aşıları ve çıplak DNA’lı aşıları içerir. Bu aşılar teorik olarak MLV aşılardan daha güvenilir olabilir. Çünkü virus üretici bir hale gelmezler. Bu aşılar aynı zamanda optimum düzeyde bir bağışıklık cevabı oluştururlar.
28. Canlı aşılar, cansız aşılara göre MDA üzerinde daha mı etkilidir?
Evet. MDA’ nın bulunduğu durumlarda bazı canlı aşılar, cansızlara göre daha erken bağışıklık gelişmesini sağlarlar.
29. Ülkemde, neden bu kılavuzdaki önerilere uygun temel aşılar bulunmuyor?
Uygun temel aşılar her ülkede mevcut değildir. Eğer sizin ülkenizde de bazı aşılar yoksa, ülkenizdeki veteriner birliklere ve siz, üretici firmalar, ve ülkenizin ruhsat veren otoriterilerine lobi yapmalısınız. Çoğu durumda, üretici firma ürünü ülkeye getirmeye meyilli olur; genelikle güçlük çıkaran taraf o ülkedeki ruhsat veren kurumdur.
30. Yerel tür (suş-strain) kullanan ilaçların uluslarası aşılara göre kullanımı daha mı uygundur?
CDV, CAV-1, CAV-2, CPV-2, FPV, FCV, FHV-1 ve kuduz hastalığına karşı geliştirilen uluslararası aşıların, iyi bir koruma oluşturmaya yeterli olmadığını gösterecek bilimsel bir kanıt bulunmamaktadır. Çoğu örnekte, kullanılan farklı türler (suş-strain), aşının temel koruyucu antijenlerini değiştirmezler. Leptospira söz konusu olduğunda ise, önemli yerel serogrupların dahil edilmesi koruyuculuğun arttırılmasını sağlar.
31. Aşıyı uygulayan veterinerler, kendilerine getirilen aşıların gerektiği gibi saklanıp kullanılabilir bir durumda olduğundan nasıl emin olur?
Uluslarası üretici firmalar, ilaçların üretimden uygulayacıya kadar nakli sırasında soğuk zinciri koruyacak sistemler kullanırlar.
32. Tetanos köpeklerde ne kadar yaygındır? Buna karşı aşı yapılmalı mıdır?
Dünyanın birçok bölgesinde köpeklerde tetanos yaygın değildir. Ruhsatı köpekler için alınmış bir tetanos aşısı bulunmamaktadır. Yüksek riskli kabul edilen bazı yerlerde, veterinerler atlar için geliştirilmiş tetonos aşısını kullanmaktadır( offlabel kullanım). Tetonosun günümüzde dünyanın birçok yerinde canine infectious hepatitis ve canine distemper’a göre daha sık görüldüğü düşünüldüğünde, köpeklere özel bir aşının geliştirilmesi açıklanabilir bir durumdur ve ticari geçerliliği vardır.
33. VGG kullanılması gereken aşı markası konusunda bir tavsiyede bulunuyor mu?
Hayır. VGG bağımsız bir akademik kurumdur, marka tavsiyesinde bulunmaz. Ancak, uluslararası kullanımı olan aşılar hakkında ciddi bir kalite, güvenlik ve etkinlik araştırması yapıldığını, bu sayede birçok ülkede ruhsat elde ettiklerini bilir. VGG, hakemli bilimsel dergilerde yapılan araştırmaların sonuçlarına göre kullanılmasında herhangi bir gereklilik ya da etkinlik olmadığı belirtilen aşıları önermez. Bu öneriler, dönemsel olarak gözden geçirilip güncellenmektedir.
34. Bir aşının Leptospira bileşeni (komponent) değil de sadece DHPPi’ si kullanacaksa, DHPPi ile birlikte ne kullanılmalıdır?
Bu soru aşının üreticisine yönetilmelidir. İyi bir çözücü steril fizyolojik veya izotonik su (sterile saline normal) veya enjeksiyon için steril su şeklinde olmalıdır. Eğer değilse, ilaç firması kullanabileceğiniz çözücüyü de vermelidir.
35. Kuduz aşısı küçük memelilerde ( tavşan, gine domuzu, vb.) de kullanılabilir mi?
VGG küçük memelilerin rutin olarak aşılanmasını önermemektedir. Bunun istisnası, gelinciktir ( ferret). Öte yandan bazı aşıların ruhsatları tüm memeliler içindir.
36. Leptospira aşısı riskli yerlerde 6 ayda bir mi kullanılmalıdır?
Yüksek riskli yerlerde, Leptospira aşısını 6 ayda bir yapmanın yılda bir aşıya göre daha fazla koruma sağladığının bilimsel dayanağı bulunmamaktadır.
37. Kuduz aşısı yapılmış bir yavru köpek, başka bir sokak köpeği tarafından ısırılırsa, PEP( post-exposure prophylaxis-bulaşma sonrası profilaksi) yapılmalı mıdır? Eğer köpeğe PEP yapılmışsa , fakat birkaç hafta sonra yeniden ısırılırsa yeniden PEP yapmak gerekir mi?
Eğer ısırılmış bir yavruya, daha önce gerektiği gibi aşı yapılmışsa, kuduza karşı koruması vardır. Bazı ülkelerde yavruya, daha çok da insanlara fayda sağlasın diye PEP yapılmaktadır. Ancak, tekrarlanan PEP’in herhangi bir faydası ispatlanmamıştır. Tekrarlanan aşılar veya enjeksiyonlar ek bir fayda sağlamamaktadır.
AŞI YAPMA PROSEDÜRÜ
38. Farklı aşıları aynı şırıngada karıştırabilir miyim?
Hayır. Eğer özel olarak belirtilmemişse, farklı aşılar bir şırıngada karıştırılmamalıdır.
39. Aynı anda farklı aşıları ( aynı ürünün parçası olmayan aşıları) bir hayvana enjekte edebilir miyim?
Evet. Ancak, aşılar hayvanın farklı lenf bezlerine yakın farklı bölgelerine yapılmalıdır.
40. Kuduz aşısı ve DHPPi aşıları aynı anda yapılabilir mi?
Evet. Aşıların birlikte kullanılabileceği bunların ruhsatlarında belirtilmediği sürece, bu uygulama offlabel bir uygulama olarak kabul edilir. İki aşının aynı zamanda kullanıldığı bir durumda, bunlar hayvanın farklı anatomik bölgelerine yapılmalıdır. Bu yolla aşı antijenleri farklı lenf bezlerine gider ve bağışıklık iki farklı noktada stimule edilmiş olur.
41. Küçük ırklarda yan etkiyi azaltmak için aşı dozunu azaltmalı mıyım?
Hayır. Üretici tarafından tavsiye edilen doz, bağışıklık oluşturacak minimum dozdur. Bu nedenle tümü uygulanmalıdır. ABD’de küçük köpekler için yeni ürünler 0.5 ml olarak formule edilmiştir. Ancak, klasik 1.0 ml aşıyla aynı miktarda antijen ve adjuvan bulundururlar. Kediler için de 0.5 ml’lik dozlar bulunmaktadır. Ancak bunların da aynı miktarda antijen ve adjuvan bulundurduğunu belirtmek gerekir.
42. Büyük ve küçük köpek ırklarına aşı aynı dozda mı yapılmalıdır?
Evet. Aşılar bağışıklık oluşturucu minimum dozlardır, ilaçlarsa vücut ağırlığıyla orantılı olarak verilir.
43. Anestezi altındaki hayvana aşı yapılır mı?
Yapmamak gerekir. Çünkü hayvan aşırı hassasiyet gösterebilir, kusabilir, solunum için risk yaratabilir. Ayrıca anestezi ajanlarının bağışıklığı değiştirebilme (immunomodulatory) özellikleri vardır.
44. Hamile hayvanlara aşı yapabilir miyim?
Prospektüste özellikle belirtilmemişse hamile hayvanlara aşı yapılmamalıdır. İzlenecek en iyi yol, çiftleştirilecek dişilerin standart aşı takvimlerini uygulamaktır. 3 yılda bir yapılacak temel aşılar yeterli düzeyde koruma sağlar. Yavru köpeklerde de yeterli derecede bağışıklık ve kolostral antikor iletilir. Çiftleşmeden ve hamile kalmadan önce ek olarak temel aşı yapmaya gerek yoktur. MLV veya cansız aşıların hamile hayvanlara uygulanmaması gerekir. Eğer hayvan barınaktaysa, ve bir salgın varsa, bu durumda aşı yapılabilir(örn. CDV veya FPV)
45. Köpek veya kedilerde immunosupresif glucocorticoid tedavisi aşının bağışıklık yaratma gücüyle etkileşime girer mi?
İki tür üzerinde yapılan araştırmalarda, bu tedavinin aşının ardından olması gereken antikor üretimi üzerinde anlamlı bir supresif etkisi olmadığı görülmüştür. Ancak, glucocorticoid tedavinin bitiminin ardından birkaç hafta sonra( en azından 2 hafta) aşı tekrarı önerilir. Özellikle eğer tedavi, temel aşılarının ilk uygulaması sırasında olduysa tekrar aşıları yapılmalıdır.
46. Bir immunosupresif -glucocoticoid dışında- veya sitotoksik(hücreler için zehirli etki taşıyan ilaç-cytotoxic) tedavi sırasında (Örn. Kanser veya otoimmün hastalıklar), aşı yapılabilir mi?
Hayır. Özellikle MLV aşıları uygulamaktan kaçınılmalıdır. Çünkü hastalığa sebep olabilirler. Cansız aşıların uygulanması etkili olmayabilir veya bağışıklık kaynaklı hastalığı arttırabilir. Yüksek dozlu ciclosporin tedavisi gören kediler üzerinde yapılan bir araştırmada, bu kedilere FPV ve FCV tekrar aşıları yapıldığında, herhangi bir bağışıklık cevabı gelişmediği görülmüştür. Aynı kedilere yapılan FHV-1, FeLV ve kuduz aşılarından sonra ise gecikmeli olarak
47. İmmunosupressif tedaviyi tamamladıktan ne kadar sonra, hayvana aşı yapılabilir?
En azından 2 hafta geçmesi gerekir.
48. Ehrlichia canis enfeksiyonu olan köpekler bağışıklıkları baskılanmış (immunosuppresed) olmalarına rağmen aşılanabilirler mi?
Monocytic ehrlichiosis’ i olan köpeklerin aşıya cevap vermeyeceği veya koruyucu antikor titrelerinin bu enfeksiyonu olan köpekte azalacağı konusunda herhangi bir kanıt yoktur. Normal izlenen yolda, ilk önce köpek tedavi edilir ve tedavi bittiğinde gerekli olan aşılar yapılır. Her durumda, kuduz aşısı yapmak yasal bir zorunluluk olabilir.
49. Hasta, hipertermik veya stres altında bir hayvana aşı yapılmalı mıdır?
Hayır. Aşıların prospektüslerinde bu durumlarda aşı yapılması tavsiye edilmez.
50. Bir hayvan yüksek risk altındaysa her hafta aşı yapabilir miyim?
Hayır. Aşılar farklı da olsalar, 2 haftadan daha sık aralıklarla yapılmamalıdır.
51. Bir yavru köpekte hiç MDA yoksa aşıya ne zaman başlanmalıdır?
Pratik olarak bir yavru köpekte hiç MDA bulunmadığını göstermek zordur. Kolostrumdan hiç faydalanmadığının bilinmesi gerekir. Ancak gerçekten bu durum biliniyorsa, temel aşılar 4 ila 6 haftalıkken yapılmaya başlanmalıdır. Bazı MLV aşılar 4 haftalıktan önce verilmemelidir, çünkü yavruda patolojiye sebep olabilirler. Eğer bu yavruda hiç MDA yoksa, 6 haftalıkken yapılacak tek bir doz aşıya olması gerektiği gibi cevap verir. Öte yandan, 16 haftalıkken 2. bir doz yapmak pragmatik bir yaklaşım olacaktır.
52.4 haftalıktan küçük yavru köpeklere aşı yapılabilir mi?
Hayır. Bu yaştaki köpeklerde bulunan MDA, MLV aşılarının bağışıklık oluşturmasına izin vermez. Ayrıca, aşıların prospektüsleri bu uygulamayı desteklememektedirler. Bu nedenle bu kadar küçük yavrulara bu aşıların uygulanması güvenli değildir. Bu duruma bir istisna, CIRDC’ye karşı olan intranazal aşıların kullanımıdır. Bu aşılar 3 haftalıktan itibaren kullanılabilir.
53. Yavru kedi ve köpeklere yapılan aşı serilerinde en son doz ne zaman verilmelidir?
Son doz 16 haftalıkken veya sonrasında verilmelidir.
54. VGG neden 12 haftalık olana kadar bazı kuduz aşılarının yapılmasını önermemektedir?
Bazı kuduz aşıları, 12 haftalıktan daha önce aşı uygulamaları için ruhsat almıştır. Eğer bu yapılıyorsa, biz 12 haftalıkken ikinci bir aşı daha yapılmasını önermekteyiz. Toplu halde yapılan aşı kampanyalarında, o bölgede bulunan mümkün olan en çok sayıda köpeğin aşılanması önemlidir. Bu nedenle, 12 haftalıktan küçük köpekler de aşılanabilir.
55. Cansız bir aşı yaptıktan kısa bir süre sonra aynı hastalık için MLV aşı da yapılabilir mi?
Hayır, cansız aşı, MLV aşıyı etkisiz hale getirecek bir antikor cevabı geliştirebilir, sonuç olarak bağışıklık oluşmasına engel olabilir. Bu nedenle, ilk önce MLV aşısı yapılmalı, eğer gerekirse cansız aşıyla tekrar aşısı yapılmalıdır.
56. İntranazal bir MLV bordetella aşısını parenteral yolla uygulayabilir miyim?
Hayır. Aşı ciddi bir lokal reaksiyona yol açabilir. Hatta sistemik hastalığa neden olarak hayvanı öldürebilir( örn böbrek iflası)
57. Parenteral yolla uygulanması gereken cansız bir bordetalla aşısını intranazal yolla uygulayabilir miyiz?
Hayır. Bu bordetallaya karşı koruyucu bir cevap oluşturmaz. Aşırı duyarlılık oluşabilir. Prospektüste belirtildiği gibi intranazal aşı burun içi yoluyla yapılmalıdır
58. Intranazal aşıdan sonra yavru köpek hapşırırsa, yeniden aşı yapmak gerekli midir?
Hapşırmayla intranazal aşının bir kısmı gidebilir. Bu aşılar, akıntıyla oluşan bir miktar kaybı tolere edecek şekilde üretilmişlerdir. Aşı hayvana hiç bir şekilde gitmediyse ya da çok az gittiyse bu durumda tekrarlamak gerekir. Aksi halde yeniden aşı yapmaya gerek yoktur.
59. Kedilere MLV FHV1 /FCV aşılarını parenteral yolla uygularken herhangi bir önlem almaya gerek var mıdır?
Evet. Ürünün mukozal( konjunktival veya nazal) temasından kaçınılmalıdır. Çünkü aşıdaki virüs hastalığa sebep olabilir. Bu temas aşının yetersiz havalandırılmasın veya kedinin aşı yapılan yeri temizlemeye çalışması sırasında aşının ordan sızması veya bulaşması ile olabilir.
60. Aşı programı sırasında farklı aşı markaları kullanabilir miyim?
Evet. Hayvanın hayatı boyunca farklı aşı markaları kullanmak doğru bir yaklaşımdır. Çünkü farklı markalardaki ürünler farklı türler (suş-strain)barındırır( örn. Feline calicivirus). Öte yandan, temel bir aşı programı sırasında farklı tür-suş bulunduran aşıları karıştırmamak gerekir( örn.FCV veya Leptospira serogrupları)
61. Temel aşılar yapılırken, farklı üreticilerin aşıları kullanılabilir mi?
Farklı uluslararası üreticilerin ürettiği temel MLV aşılar içerik bakımından benzeşir ve temel aşıların ilk uygulaması sırasında farklı markalar uygulanabilir( örneğin bir 8-9 haftalık yavru köpeğe ilk aşı bir veterinerde yapılır, ikinci aşı farklı bir veterinerde farklı bir markalı ürünle yapılır). Üreticiler bu uygulamaya karşıdırlar, çünkü ürünlerinin diğer marka aşılarla olan uyumunu araştırmamışlardır. Temel olmayan aşıların farklı markalardan olması kabul edilebilir bir uygulamadır. Bunun istisnası Leptospiradır. Çünkü ilk doz 2 serogrup içeren bir aşıyla yapıldığında, eğer ikinci doz 4 serogrup içeren başka bir aşıyla yapılırsa, bu aşılar bir bağışıklık oluşturmaz. Aynı durum FCV aşıları için de geçerlidir.( 60. Soru cevaba bakınız)
62. Aşı öncesi, aşı yapılacak alanı dezenfektanla( alkol) temizlemek gerekir mi?
Hayır. Dezenfektanın uygulamak MLV aşıyı etkisiz hale getirebilir.
63. Karışım halindeki aşıları bölebilir miyim?
Evet. Örneğin, leptospira bakterili aşısı viral antijen karışımlarında çözücü olarak kullanılır. Viral kek olarak adlandırılan bu ürün, steril suda veya tampon çözeltide(buffered saline) çözülebilir. Leptospira bakterili aşısı ise ayrı olarak hayvanın başka bir bölgesine yapılabilir, veya daha sonra yapılmak üzere kaldırılabilir.
64. Tek doz olarak yapılan aşılar kedi veya köpeğe bir fayda sağlar mı? Kedi ve köpek popülasyonu bundan faydalanır mı?
Evet. 16 hafta veya sonrasında bir doz MLV aşısı ( CDV, CPV-2 CAV-2 veya FPV ) yapılan kedi veya köpeklerde uzun süreli bağışıklık oluşur. 16 haftalık veya daha büyük her yavru kedi ve köpeğe bir doz MLV temel aşısı yapılmalıdır. Kediler için olan temel solunum yolları aşıları ( FCV ve FHV-1) söz konusu olduğunda bunları 2-4 haftalık aralıkta 2 doz olarak uygulamak korumayı en üst düzeye çıkarır.
Eğer bu yol izlenirse, hayvan popülasyonu bağışıklığı anlamlı bir şekilde iyileştirilir. Yüksek aşılama oranlarının olduğu ABD’ de bile yavru köpeklerin aşı oranı % 50’ den düşükken, yavru kedilerin de % 25’ ten düşüktür. Eğer temel aşılarla daha fazla hayvan aşılarsak( en azından popülasyonun % 75’i) popülasyon bağışıklığı elde edilir ve salgın hastalıklardan korunulur.
65. Bağışıklık oluşturması için ( örneğin leptospira bakterileri, veya feline leukaemia virüsü) iki doz yapılması gereken bir aşının ikinci dozu izleyen 6 hafta içinde yapılmıyorsa, bağışıklık oluşur mu?
Hayır. İki dozlu aşıların tek doz yapılması bağışıklık oluşturmaz. İlk doz bağışıklık sitemini hazır hale getirirken, ikinci doz bağışıklık oluşturur. Eğer ikinci doz 6 hafta içinde yapılmazsa, aşıya sıfırdan başlanmalıdır. Bu sefer, iki aşının arasının 2-6 hafta olması gözetilmelidir. İki doz aşı tamamlandıktan sonra, tekrar aşıları 1 yıl veya daha fazla aralıklarla yapılabilir.
66. Sulandırılmış MLV aşısı oda sıcaklığında ne kadar süre etkinliğini kaybetmeden kalabilir?
Çok hassas olan bazı MLV aşılar ( CDV, FHV-1) bağışıklık oluşturma özelliklerini oda sıcaklığında 2-3 saat kaldıklarında kaybederler. Bazı farklı içerikli MLV aşılarsa, bir kaç gün kalsalar da bağışıklık oluşturabilirler( örn. CPV, FPV). VGG, oda sıcaklığındaki MLV aşıların 1-2 saat içinde kullanılmalarını önermektedir.
67. Temel aşıda minimum koruma süresi geçirilip (CDV, CPV-2, CAV-2 için 7-9 yıl, FPV için 7 yıl) aşı yapılmamışsa, aşı serilerine yeniden başlamak gerekir mi (2-4 hafta aralıklarla birkaç doz)?
Hayır. MLV aşıları birkaç doz olarak yapmak MDA’ sı olan yavrular için söz konusudur. VGG birçok aşı prospektüsünde aşı serilerine yeniden başlanmanın önerildiğini bilmektedir. Ancak bu öneriler, temel bağışıklık sistemi çalışma prensiplerine ve bağışıklık hafızası presiplerine aykırıdır.
68. FeLV ve/ veya FIV enfeksiyonları olan bir kedi aşılanmalı mi?
FeLV veya FIV pozitif olan bir kedinin, klinik bulguları iyiyse, riski minimize etmek için evde diğer kedilerden uzakta yaşamalıdır. Eğer temel aşıların yapılması gerekiyorsa (FPV, FCV ve FHV-1) , uzmanlar bunun cansız aşılarla olmasını önermektedir. Bu kedilere FeLV ve FIV’e karşı aşı yapılmamalıdır. FeLVveya FIV pozitif olan kedi klinik olarak hasta gözüküyorsa aşı yapılmamalıdır. Bazı ülkelerde retro virusle enfekte kedilere kuduz aşısının yapılması bir zorunluluktur.
69. Aşı kedilerin hangi bölgelerine yapılmalıdır?
Kedi aşıları( özellikle adjuvanlı olanlar) interskapular bölgeye yapılmamalıdır. ABD’de kuduz aşıları, distal sağ arka bacağa, felv aşıları sol arka bavağa, temel fpv, FCV ve fhv-1 aşıları ise distal ön bacaklara yapılmaktadır. Deri altına yapılan aşılarda bir diğer alternatifse, distal kuyruk veya lateral göğüs veya abdominal duvara enjeksiyonlardır. Bu yollardan bu kitapçığın ilgili bölümünde bahsedilmiştir. Hangi bölge seçilirse seçilsin, aşı deri altına yapılmalıdır, kasiçi olmamalıdır. Aşı yapılan bölgeler her seferinde değiştirilmelidir. Bunu sağlamak için de aşı yapılan bölgeler her seferinde kaydedilebilir, bunlar her aşıda değiştirilebilir.
70. Ciddi beslenme yetersizliği aşıyla bağışıklık geliştirmeyi etkiler mi?
Evet. Ciddi beslenme yetersizliği sonucu oluşan vitamin ve mineral eksikliğinin( vitamin E/ selenium) yavru köpeklerde koruyucu bağışıklığın gelişmesine engel olabileceği yapılan araştırmalarda gösterilmiştir. Şüphelenilen ya da bilinen beslenme yetersizlikleri yapılan takviyelerle giderilmelidir. Daha sonra hayvan yeniden aşılanarak koruyucu bağışıklığın oluşması sağlanmalıdır.
71. Eğer yavru bir kedi veya köpek annesinden kolostrum almazsa, anneden geçen başka bir pasif bağışıklık kaynağı var mıdır?
Annenin antikor titresine bağlı olarak çok az ya da hiç koruyucu bağışıklık olmayacaktır. Çünkü yeni doğmuş hayvandaki pasif antikorların % 95’ i kolostrumdan geçer ve doğumdan sonra en geç 24 saat içinde bağırsak yoluyla emildiği gözlenir.
72. Kolostrum almamış yavru bir kedi veya köpekte MDA bulunmadığına göre, ilk haftalarda aşı yapılabilir mi?
Hayır. 4-6 haftadan küçük yavrulara MLV aşıları yapılmamalıdır. Bazı MLV aşılar 2 haftadan küçük MDA’sı olmayan yavrulara yapıldığında, hayvanın merkezi sinir sistemininde enfeksiyona sebep olup ölümüne yol açabilir. Bunun sebebi yavrularda ilk haftalarda vücut sıcaklığını düzenleyecek ve kontrol aldında tutacak sistemin gelişmemiş olması ve aşının adaptif bağışıklığa zarar vermesidir.
73. Kolostrum alamamış genç hayvanlar temel hastalıklardan nasıl korunur?
1 günlükten küçük hayvanlara yapay kolostrum verilebilir. Yapay kolostrum şu şekilde elde edilebilir: % 50 süt yerine geçen ürün( örneğin Esbilac veya yerine geçen başka bir ürün) % 50 bağışıklık serumu( anneden veya anneyle aynı yerde yaşayan aşıları tam ve herhangi bir enfeksiyonu olmayan bir hayvandan elde edilmiş olması tercih edilir). Eğer yavrular 1 günlükten büyükse, bağışıklığı tam olan yetişkin bir hayvandan alınan serum deri altına veya intraperitoneal olarak yapılabilir; ya da sitratlı plazma damar içi yolla uygulanabilir. Hayvanın büyüklüğüne göre, günde 2 kez, 3 güne kadar, 3 ila 10 ml serum veya plazma uygulanabilir.
74. Hangi yaştaki köpeklerin artık aşılanmasına gerek yoktur?
Temel aşılar söz konusu olduğunda, 3 yıldan sık olmamak kaydıyla tüm hayatları boyu aşı yapılması önerilmektedir. Temel hastalıklara (örn. CDV, CAV and CPV-2) karşı korumanın devam edip etmediği yapılacak serolojik testlerle belirlenebilir. Serolojik testlerin 3 yılda bir yapılması önerilmektedir.10 yaşından büyük köpekler için her sene yapılması önerilir. Birçok ülkede kuduz aşısının belirlenen aralıklarda yapılması yasal bir zorunluluktur.
75. Hiç aşı yapılmamış yetişkin bir köpek için uygulanması gereken aşı protokolü nasıldır?
Temel aşılar tek doz MLV olarak uygulanmalıdır (CDV, CAV-2, CPV-2). Risk bulunan bölgelerde kuduz aşısı da yapılmalıdır. Bu aşıları 2 doz yapmaya gerek yoktur. Tekrar aşılarının (veya CDV, CAV ve CPV-2 için serolojik test) 3 seneden erken yapılmasına gerek yoktur. Temel olmayan aşılar yapılacak risk fayda analizine göre belirlenmelidir. Belirlenecek temel aşıların 2-4 hafta aralıklarda 2 doz olarak yapılması gerekir.
76. Leptospira hastalık geçmişi bilinmeyen yetişkin bir köpek için önerilen aşı protokolü nedir? Yavru köpekler için olduğu gibi 2-4 haftalık aralıklarla 2 doz mudur?
Evet. Köpeğe 2-4 haftalık aralıkta 2 doz aşı yapılmalıdır. Ondan sonra her sene aşı tekrarlanmalıdır.
77. Aşısı olmayan yetişkin bir kedi için hangi protokol önerilmektedir?
VGG, hiç aşı yapılmamış yetişkin bir kediye 2 doz temel MLV aşısı (FPV, FCV, FHV-1) ve kuduzun yaygın olduğu bölgelerde 1 doz kuduz aşısı yapılmasını önermektedir. FPV söz konusu olduğunda düşük riskli bir kedi için tekrar aşılarının( veya FPV için serolojik test) 3 yıldan önce yapılmasına gerek yoktur. Yüksek riskli kediler için FHV-1ve FCV aşıları her sene yapılmalıdır. Temel olmayan aşılar risk fayda analizi sonucuna göre belirlenmelidir.
78. Üst solunum yolu hastalık belirtileri görülen bir kediye aşı yapılmalı mıdır?
Hasta bir kediye aşı yapılmamalıdır. İyileştiğinde, FCV veya FHV (eğer ikisi de solunum yolu hastalığına sebep olduysa iki aşı da yapılabilir) ye karşı doğal bir bağışıklık geliştirmiş olurlar. Ancak oluşan bağïşıklık aşılardan sonra olmasına rağmen mikroplardan arındıramaz. Viral bir solunum yolları hastalığı geçirip iyileşmiş bir kedinin aşılanmaması gerektiğine dair bir endikasyon YOKtur. Trivalan bir aşı FPV’ye karşı koruduğu gibi daha önce hayvanda hastalık oluşturmamış solunum yolları hastalıkları viruslerine karşı da (FHV-1 ve FCV)koruma sağlar.
79. 2-3 gün süren elektrik kesintileri olduğunda buzdolabındaki aşılar ne yapılmalıdır? Kullanılabilir mi?
2-3 gün boyunca uygun sıcaklıkta saklanmamış MLV aşıları kullanılmamalıdır. Bu aşıların bazı bileşenleri( örn. CDV) ısıya duyarlıdır ve virusler inaktif hale gelebilirler. Şüpheli durumlarda üreticiden bilgi alınmalıdır.
SEROLOJİK TESTLER HAKKINDAKİ SORULAR
80. Serumdaki antikor titreleri aşı kaynaklı bağışıklığı tanımlamakta faydalı mıdır?
Evet. Özellikle köpeklere uygulanan CDV, CPV-2 ve CAV1 ve kedilere uygulanan FPV ve yasal amaçlarla yapılan kuduz aşısından sonra yapılabilir. Diğer aşılarda serumdaki antikor titrelerine bakmanın bir anlamı yoktur. Çeşitli aşılar için yapılan CMI(antikorlar dışında başka faktörlerle aktive edilen bağışıklık) deneylerin de teknik ve biolijik açıdan bir faydası tespit edilmemiştir. Laboratuvarın kalite güvencesine bağlı olarak birbirinden farklı sonuçlar elde edilebilmektedir.
81. Klinikte yapılan testlerde, CPV-2/CDV aşıları yapıldıktan sonra koruyucu antikor konsantrasyonlarını ölçmeden önce ne kadar süre beklemek gerekir?
Bu soru yavrular için geçerlidir, çünkü yetişkin köpeklerde tekrar aşısının yapıldığı sırada, en son aşının yapıldığı zamandan bağımsız olarak zaten serum antikorları mevcuttur. Eğer bir yavruya aşının son dozu 16 haftalıkken uygulanırsa, 20. haftadan sonra test yapılabilir. Test sonucunda bulunan antikorlar, yavrunun aktif olarak korunduğunu gösterir.
82. VGG neden rutin olarak kuduz antikor testi yapmayı tavsiye etmemektedir?
Birçok ülkede titre sonuçlarından bağımsız olarak, köpeklere rutin olarak kuduz aşısı yapılması yasal bir zorunluluktur. Bu nedenle bu sorunun cevabının çoğu veteriner için bir anlamı bulunmamaktadır. Kuduz antikor testi, evcil hayvanların uluslarası seyahati söz konusu olduğunda istenmektedir. Uluslararası kuduz aşısı yüksek derecede etkindir, ve genellikle aşıyı takiben bağışıklık oluştuğunu göstermeye gerek yoktur.
83. CDV, CPV-2 ve CAV söz konusu olduğunda, MDA’ yı test etmek ve ilk aşı zamanına karar vermek için antikor testleri kullanabilir miyiz?
Teorik olarak bu mümkündür. Yıllar önce anne köpeğin serumundaki antikorların titresi nomogram kullanarak yavru köpeğin aşı zamanının belirlenmesi için kullanılıyordu. Pratikte, yavrularda MDA’ nın seyrini takip etmek için devamlı surette kan testi uygulamak hem zor hem de pahalıdır
84. Aşının üzerinden 3 sene geçtikten sonra, antikor titreleri ne durumdadır?
CDV, CAV-2, CPV-2 ve FPV aşılarında antikor titreleri hep aynı düzeyde bulunacaklardır. Bu, köpekler üzerinde yapılan bir çok saha araştırmasında gösterilmiştir: en son 9 sene önce aşılanmış ve en son 14 sene önce aşı yapılmış köpekler üzerinde yapılan araştırmalarda, Leptospira titreleri aşıdan kısa bir süre sonra düştüğü ve korumayla doğru bir korelasyon izlmediği görülmüştür. FCV ve FHV-1 için serum antikor titreleri daha az geçerlidir, çünkü bunlarda en önemli bağışıklık mukozal ve hücresel bazda oluşur.
85. Yavruyken aşıları tamamlanmış bir hayvanda, önemli hastalıklara karşı koruma sağlanması için antikorların yüksek titrede mi olması gerekir?
CDV, CAV-2, CPV-2 ve FPV için cevap hayırdır. Titre miktarından bağımsız olarak, antikorların varlığı koruyucu bağışıklığın olduğunun göstergesidir. Antikor titrelerini arttırmak için olması gerektiğinden daha sık yapılan aşılar faydasızdır. Antikor titre miktarını arttırarak daha fazla bağışıklık sağlamak mümkün değildir.
86. Yıllık aşıya bir alternatif olarak köpeklere test uygulayabilir miyiz?
Evet tabii ki. Şu anda CDV, CAV, CPV-2 ve FPV aşıları için özel tasarlanmış ve koruyucu serum antikorlarını gösteren ve geçerliliği kanıtlanmış test kitleri bulunmaktadır. Bazı ülkelerde bu testler, 3 yıllık aralıklarla yapılan temel aşıların koruyuculuğunun belirlenmesinde kullanılmaktadır( otomatik olarak 3 yılda bir aşıları tekrarlamak yerine). Serolojik testler her sene yapılabilir, ancak bu test sonuçları incelendiğinde her sene test yapmanın gereksiz olduğu sonucuna ulaşılır.
YILLIK SAĞLIK KONTROLÜ
87. Yıllık sağlık kontrolü sırasında hangi testler veya kontroller yapılmalıdır?
Yıllık kontrolü sırasında, temel fiziksel kontroller yapılmalıdır (ateş, kalp atışlarının dinlenmesi, vücudun elle muayenesi). Hasta sahibinden, muhtemel riskleri belirlemek için hayvanın yaşam biçimi hakkında bilgi alınmalıdır(örn.yaptığı seyahatler, evin içinde ve dışında bulunması vs.) beslenme şekli ve parazit kontrolüyle ilgili hayvan sahibinden bilgi alınmalıdır. Bazı ülkelerde yaygın enfeksiyonel hastalıklara karşı rutin testler de yapılmaktadır.
88. Bazı hayvan sahipleri sadece yıllık kontrol için veterinere gitmeye karşı olabilirler. Bu durumda, hayvan sahibini ikna edebilmek için neler yapılmalıdır?
Bu durum hayvan sahibinin bilgilendirilmesi ile ilgilidir. Müşterilere bu kontrollerin hayvanlarının sağlığını olumlu yönde etkilediği ve erken teşhise olanak verdiği anlatılmalıdır. Aşı açısından ele aldığımızda, sağlık kontrolü sırasında temel aşılardan 3 yıllık süreyi dolduranlar için kan testi ve temel olmayan aşılar gerekliyse bunlar yapılabilir.
89. Hastalarım yıllık sağlık kontrolünü çok pahalı buluyor.
Yıllık sağlık kontrolü hayvana yapılan tam bir fiziksel kontrol veya klinik geçmişinin incelenmesi kadar basit olmalıdır. Bunların ücreti veterinerin bu kontroller için harcadığı zamanın karşılığı dikkate alınarak belirlenmelidir. Esas olarak, yıllık sağlık kontrolü kavramı daha önce de yapılan yıllık aşı tekrarı ve fiziksel muayenesinin yeni yoludur. Daha zengin müşteriler içinse yeni veterinerlik hizmetleri sunmak ve uygulamanın faydasını arttırmak için bir yoldur. Aynı zamanda daha iyi hizmet sunmak ve müşteri veteriner ilişkisini geliştirmek için bir imkan sunar.
AŞILARIN YAN ETKİLERİYLE İLGİLİ SORULAR
90. Bir hayvana gereğinden fazla aşı yapmak risk oluşturur mu?
Evet. Aşılar gerekmedikçe yapılmamalıdır, yan etkiye yol açabilirler. Aşılar, her hayvan için bireysel bazda ele alınması gereken medikal ürünlerdir.
91. Bazı aşılarda diğerlerine göre yan etki görülme olasılığı daha mı fazladır?
Genellikle böyle düşünülse de, bunu destekleyen bilimsel kanıtlar çok azdır. Yan etki görülmesi, genellikle hayvanın genetiğine bağlıdır.( örn. Küçük ırk hayvanlar) (Moore ve diğerleri 2005, Kennedy ve diğerleri 2007). Leptospira, Bordetella, Borrelia ve Chlamydia gibi bakterili aşıların (cansız bakterili aşılar) , MLV viral aşılara göre daha fazla tip 1 aşırı duyarlılığa neden olduğu düşünülmektedir. Ancak bunu destekleyici kanıtlar bulunmamaktadır. Adjuvanlı FeLV ve kuduz aşılarının kedilerde sarkomaya neden olduğu düşünülse de, bu konuda çelişkili sonuçlar bulunmaktadır.
92. Daha önce aşıya karşı yan etki görülmüş ya da bağışıklık nedenli hastalık görülmüş kedi ve köpeklere( örn.ürtiker, yüzde ödem, anaflaksi, enjeksiyona bağlı sarkoma, otoimmun hastalık gibi) aşı yapılabilir mi?
Eğer yan etki görülen aşı, temel bir aşıysa, serolojik bir test yapılıp, seropozitif ( CDV, CAV, CPV-2, FPV)çıkan hayvanlara aşı yapılmasına gerek yoktur. Eğer aşı tercihe bağlı temel olmayan bir aşıysa( örn.Leptospira veya Bordetella bakterili aşısı) aşı yapılması tavsiye edilmez. Kuduz aşısı söz konusu olduğunda, resmi kurumlara danışılıp, aşı yapılmasının gerekliliği sorgulanmalı, antikor titrelerine bakmanın yeterli olup olmadığı araştırılmalıdır.
Eğer aşı yapılması mutlaka gerekliyse, marka-üretici değiştirmek faydalı olabilir. Ancak bu yol her zaman başarılı olmayabilir, çünkü aşırı duyarlılığın, ilaçlarda kullanılan katkı maddesine( eksipiyan) bağlı olduğu bilinmektedir( örneğin virus üretiminde kullanılan bovine serum albumin). Aşıdan önce antihistaminik veya antienflamatuar glucocorticoidler kullanılabilir, aşının tutmasına engel olmazlar. Yeniden aşı yapılmış hayvanlar, oluşabilecek yan etkilere karşı aşıyı takip eden 24 saat boyunca yakından takip edilmelidir. Tip 1 aşırı duyarlılık aşıyı takip eden birkaç dakika içinde kendini gösterebilir; diğer tiplerdeki aşırı duyarlılık(2,3,4) daha sonra da görülebilir (Bu süre saatlerden aylara kadar değişir).
93. Genellikle küçük ırk köpeklerde aşıdan sonra yan etkiler görülmektedir. Bunu engellemek için, aşının dozunu azaltabilir miyiz?
Hayır. Aşıların dozu, ilaçlarda olduğu gibi mg/ kg hesabına bağlı değildir. Bağışıklık oluşması için tüm antijenli yükün alınması gerekmektedir. Aşı dozları, küçük köpeklere verilirken bölünmemeli, ya da azaltılmamalıdır. ABD’ de küçük köpekler için 0.5 ml lik dozdayeni bir aşı üretilmiştir. Ancak 1.0 ml lik aşı kadar antijen ve adjuvan bulundurmaktadır. Bu nedenle küçük ırklarda görülen yan etkileri azaltması beklenmemelidir. Bu ve diğer aşılar, günümüzde artık, eksipiyan( yardımcı madde) konsantrasyonları daha düşük orandadır(92. Soru cevaba bakınız). Dış kaynaklı (extraneous) protein konsantrasyonunun düşürülmesi görülen yan etkileri azaltmaktadır.
94. Aşılar otoimmün hastalıklara sebep olabilir mi?
Aşılar tek başlarına böyle bir şeye sebep olmazlar. Ancak genetik olarak yatkın hayvanlarda, hastalıkla takip edilen otoimun reaksiyonlar görülebilir( herhangi bir enfeksiyon, ilaç veya çevresel faktörlerin neden olduğu durumlar gibi).
95. Aşıdan sonra yan etkiler ne kadar sık görülür?
Sağlıklı bilgi edinmek zor olduğundan bu sorunun kesin cevabını söylemek zordur. Yan etkilerin sıklığının belirlenebilmesi için hayvan sahibinin ya da veterinerin görülen yan etkileri üretici firma ya da yetkili kurumlara bildirmesi gereklidir. Günümüzde kullanılan aşıların çok düşük oranda yan etkiye yol açtığı kabul edilmektedir. Aşının hastalıklara karşı sağladığı fayda görülebilecek yan etkilerin riski yanında ağır basmaktadır. Amerikada yakın tarihte, çok yüksek sayıda aşılanmış kedi ve köpeklerle ilgili bilgiler incelenmiştir. Köpeklerde aşıyı izleyen 3 günde, 10000’ de 38 oranında yan etki ( çok küçük yan etkiler de dahil edilmiştir) gözlemlenmiştir (Moore ve diğerleri, 2005). Aşı yapılan 10000 kediden 52’ sinde de aşıyı takip eden 30 günde yan etkiler görülmüştür. (Moore ve diğerleri, 2007). Ancak raporlanmayan reaksiyonlar da görülmüş olabilir, ya da başka bir veterinere raporlanan reaksiyonlar da gelişmiş olabilir. Bazı ırk hayvanlarda diğerlerine göre daha yüksek oranda yan etki görülme olasılığı bulunmaktadır.
96. Aşı sonrası bağışıklık oluşmayan kedi ve köpekler var mıdır?
Evet. Bu durum, bazı ırklarda görülen genetik bir özelliktir. Bu özelliği taşıyan aynı aileden veya ırktan hayvanlarda görülür. Eğer canine parvovirus veya feline panleukopenia gibi aşılara cevap vermeyen bir hayvansa, bu enfeksiyonları kaptığında ölebilir. Eğer ölüme yol açmayan bir patojene karşı hassas bir hayvansa, hayvan hastalanabilir, ancak ölmez (örn Bordetella bronchiseptica enfeksiyonundan sonra).
97. Yavru köpeklere yapılan ilk seri aşılardan sonra immunosupresyon gelişir mi?
Evet. Eğer MLV-CDV ve MLV-CAV-2 den oluşan bir karışım verilirse, aşıdan 3 gün sonra , 1 haftaya kadar immunosupresyon gelişebilir (Strasser ve diğerleri 2003). Bu aşının normal sonuçlarından biridir, nadiren de olsa bazen klinik sorunlar görülebilir. Eğer kombine edilen aşı MLV-CDV veya MLV-CAV-2 bulundurmazsa, immunusupresyon meydana gelmez.
98. Yavru köpeklerin hepsine temel aşıların yapılması gerekir. Immunosupresyon olmaması için ne yapmak gerekir?
Yavrulara parenteral yoldan CDV ve CPV-2 içeren bivalan bir aşı yapılabilir. Cav-2 de daha sonra yapılabilir.
99. Bazı cins köpeklerde Leptospiraya karşı oluşan bağışıklık cevabı sırasında aşırı duyarlılık oluşur. Bu yan etki de aşının oluşturduğu bağışıklık gibi kısa süreli midir (1 yıldan kısa)?
Hayır. Bağışıklık ve IgG hafızasının tersine (≤1 yıl), aşı sonrası oluşan aşırı duyarlılık hafızası uzun sürelidir(≥4 yıl).
100. Aşılara karşı oluşan hafif bir alerjik reaksiyon steroidle tedavi edilebilir mi?
Evet. Yüz ödemi, pruritus gibi reaksiyonlar oral cocorticoidlerin (örn. Prednisolone) antienflamatuar dozlarıyla ve antihistaminiklerle tedavi edilebilir.
101. Kütanöz vaskülitlerin aşı yüzünden oluştuğu doğru mu?
Evet. Bu aşıdan sonra çok nadir görülen bir reaksiyondur. Özellikle kuduz aşısından sonra görülür.
102. Kedilerde de köpeklerde olduğu gibi aşılara karşı gelişen kütanöz alerjik reaksiyonlar görülür mü?
Evet. Kedilerde de aşıyı takiben köpeklerde olduğu gibi tip 1 aşırı duyarlılık belirtileri görülebilir ( ör. Yüz ödemi, kütanöz pruritus).
103. Kedilerde görülen sarkomanın sebebinin aşı olduğunu nasıl anlarız? Bu sarkomalarla ilgili ne yapılabilir?
FISS (feline injection site sarcoma) daha önce enjeksiyon yapılmış anatomik bir bölgede ortaya çıkar. Bu tümörlere aşıların da dahil olduğu enjekte edilebilen maddelerin sebep olduğu düşünülmektedir. Kedilere yapılan aşıların anatomik bölgelerinin kaydının alınması tavsiye edilmektedir. Ayrıca Wsava kılavuzu kedilerde aşı yapılacak bölgeler üzerine de tavsiyede bulunmaktadır. Kediler için mümkün olduğunda adjuvansız aşılar seçilmelidir. Maalesef bu sarkomalar çok agresif yapıdadırlar. Vücuda yayılıp, % 20 oranında metastaz oluştururlar. Bir uzman tarafından yapılacak cerrahi bir müdahale, daha sonra da radyoterapi ve immünoterapi gerekebilir.
104. Neden şimdi eskiye göre, kuduz aşılarından sonra daha fazla aşırı duyarlılık görülmektedir? Neden bu durum toy poddle ırkında daha sık görülür?
Aşırı duyarlılık her tür aşı yüzünden olabilir. Aşılara üretimleri sırasında konulan Bovine Serum Albumin(BSA) adlı antijenin bu reaksiyonlara sebep olduğu bilinmektedir. Üreticiler, hayvanlara uygulanan aşılarda BSA miktarını azaltmaya çalışmaktadırlar. Bu reaksiyonlar bazı “oyuncak ırklarda” daha sık görülmektedir(Miyaji ve diğerleri 2012). Genetik bir hassasiyet olduğu düşünülse de, nedeni kesin olarak bilinmemektedir.
105. Neden bazı üretim/çiftleştirme merkezlerinde CDV ve CPV-2 enfeksiyonları yüzünden ölen köpekler sık görülmektedir?
Bu durumun en olası sebebi çiftleştirilecek hayvanların aşılarının iyi bir şekilde yapılmamasıdır. Anneler etkin bir şekilde aşılanmadığı için, yeterli miktarda MDA olmayan yavrular arasında salgın gelişebilir. Öte yandan, WSAVA kılavuzuna göre aşıları yapılamamış yavruların da ( örn. Son doz aşının 16 haftalıkken veya sonrasında yapılması gerekliliği), eğer anneden geçen antikorlar düşük seviyedeyse, korumasız kalma riski bulunmaktadır. Son olarak, Rottweiler, Dobermann gibi genetik olarak aşılara cevap veremeyen ırklarda bağışıklık gelişmeme riski bulunmaktadır. İyi bir şekilde hayvan yetiştiriciliği yapmak, hijyen ve iyi beslenme bu riskleri minimize etmede önemli bir rol oynar.
106. MLV aşı virulansa dönüşebilir mi?MLV aşısı yapılmış bir köpek enfekte olur mu?
Evet. MLV aşı virulansa dönüşebilir, ama bu çok nadir bir durumdur. Aşılara ruhsat verilirken, üreticilerden aşıdaki virüsün yayılmayacağını kanıtlamaları istenir. MLV aşılar enfeksiyonlu aşılar olarak adlandırılırlar, çünkü bağışıklık için düşük derecede bir enfeksiyon oluşturarak koruma sağlarlar. Ancak hastalık oluşturmazlar. Canine parvovirus söz konusu olduğunda MLV aşı yapılan köpekler, aşıyı takip eden kısa bir süre dışkılarında virus yayarlar. Ancak bu diğer köpekler için bir risk teşkil etmez.
107. Neden bazı köpeklere 6 haftalıkken dHPPİ aşısı yapıldığı halde 7 haftalıkken parvovirus enfeksiyonu görülür?
Aşı yapılmış bir yavruda enfeksiyon görülmesinin başlıca sebebi, bu hayvanda aşı yapıldığı sırada zaten bir enfeksiyon olmasıdır. Hayvanın hassas dönem(window of susceptibility) denilen dönemde de hastalanması mümkündür. Bu dönemde vücudundaki MDA’lar tam koruma sağlamak için yetersizken, yeni yapılmış bir aşının tutmasını engelleyecek seviyededir.
108. Yıllık aşı tekrarlarının, az sayıdaki yan etkileri dışında başka riskleri var mı?
Aşının yan etkileri son derece azdır. Kedi ve köpeklerde, aşı yapılan her 10000 hayvandan 30 ila 50 tanesinde yan etki görülür. Bu görülen yan etkilerin büyük kısmı da ciddi olmayan reaksiyonlardır( örn. Kısa süreli ateş ve letarji, alerjik reaksiyonlar). Yeni aşı yapma kılavuzunu geliştirmenin amacı, sadece riskleri azaltmak değil, aynı zamanda kanıta dayalı daha iyi veterinerlik uygulamalarında bulunmak, ve sadece gerektiğinde bir medikal uygulama yapmaktır.
109. Bazı köpekler ( örn. Rottweiler) genetik olarak aşıya iyi cevap vermiyorlar.Bu köpeklere nasıl aşı yapılmalıdır?
WSAVA aşı klavuzunda bulunan akış diagramı, aşıya cevap vermeyen köpeklerin tespit edilmesinde kullanılabilir. Tüm yavru köpekler aynı şekilde, daha önce yukarıda belirtildiği gibi aşılanmalıdır ( son aşı 16 haftalıkken veya sonrasında yapılmalıdır). Eğer aşının tutmadığından şüpheleniliyorsa, 20 haftalıkken serolojik test yapılmalıdır. Genellikle cevap vermeyen köpeklerin çoğunda, sadece bir temel aşının antijenlerine karşı seroconversiyon çıkmayacaktır( örn. CDV, CAV, CPV-2). Bu köpekler yeniden aşılanıp, yeniden test yapılabilir. Ama gerçek anlamda cevap vermeyen bir köpekte, yine bağışıklık oluşmayacaktır. Bu hayvanlar, bu antijene karşı bağışıklık geliştirme kapasitesine sahip değildirler, ve bunlarda bu aşı hiçbir zaman tutmaz. Sahipleri bu köpekleri risk altında kabul edip, çiftleştirmede kullanmamalıdır.
110. Aşının risk fayda analizini nasıl yapmalıyız?
Risk fayda analizi sadece temel olmayan aşılarda söz konusudur. Tüm kedi ve köpekler, yaşadıkları şartlardan bağımsız olarak temel aşılarla aşılanmalıdır( kuduzun yaygın olduğu yerlerde kuduz aşısı da temel aşılara dahil edilmiştir.). Risk fayda analizi her hayvanda bireysel bazda yapılır. Sahibinin size, nerde yaşadığı( içerde mi dışarda mı), seyahat, diğer hayvanlarla aynı ortamı paylaşma sıklığı gibi konularda verdiği bilgiler doğrultusunda analiz yapılır. Dikkate alınması gereken riskler: 1. Aşıyı takip eden yan etkiler, 2. Gereksiz bir medikal uygulama yapma riski, 3. Bölgenizde olduğu bilinen bir enfeksiyonu kapma riski, 4. Bu enfeksiyonu takip eden bir klinik hastalık oluşması riski. Olası faydalar ise: 1. Yaşam tarzı ve bulunduğu coğrafya dolayısıyla risk altındaki hayvanın, enfeksiyondan aşı sayesinde korunması,2. Hayvan enfekte olduğunda aşı enfeksiyonun klinik belirtilerinin ciddi seyretmesine engel olur. 3.Aşıyla , tüm popülasyon enfeksiyondan korunur.
111. Hayvanlarınıza aşı yaptırmak yerine aşıların çalıştığını algılayacak antikor speed testlerinin yapılması hayvanınız için çok daha sağılıklıdır.
Testler pozitif verdiği durumlarda aşı yerine beklemek ve gelecek yıl aşı yaptırmak onların aşı yükünden kurtulmalarını sağlamaktadır.
REFERANSLAR
- Anderson, T. C., Crawford, P. C., Dubovi, E. J. et al. (2013) Prevalence of and exposure factors for seropositivity to H3N8 canine influenza virus in dogs with influenza- like illness in the United States. Journal of the American Veterinary Medical Association 242, 209-216
- Anon. (2013a) Survey suggests many pets do not receive preventive healthcare. Veterinary Record 172, 569
- Anon. (2013b) WSAVA and OIE call for action on rabies. Veterinary Record 173, 463-464
- Arjona, A., Barquero, N., Domenech, A et al. (2007) Evaluation of a novel nested PCR for the routine diagnosis of feline leukemia virus (FeLV) and feline immunodeficiency virus (FIV). Journal of Feline Medicine and Surgery 9, 14-22
- AVSAB (American Veterinary Society of Animal Behavior) (2008) Position statement on puppy socialization.
- Bande, F., Arshad, S. S., Hassan, L. et al. (2012) Prevalence and risk factors of feline leukaemia virus and feline immunodeficiency virus in peninsular Malaysia. BMC Veterinary Research 8, 33
- Bandecchi, P., Matteucci, D., Baldinotti, F. et al. (1992) Prevalence of feline immunodeficiency virus and other retroviral infections in sick cats in Italy. Veterinary Immunology and Immunopathology 31, 337-345
- Beczkowski, P. M., Harris, M., Techakriengkrai, N. et al. (2015a) Neutralising antibody response in domestic cats immunised with a commercial feline immunodeficiency virus (FIV) vaccine. Vaccine 33, 977-984
- Beczkowski, P. M., Litster, A., Lin, T. L. et al. (2015b) Contrasting clinical outcomes in two cohorts of cats naturally infected with feline immunodeficiency virus (FIV). Veterinary Microbiology 176, 50-60
- Bennett, M., McCracken, C., Lutz, H. et al. (1989) Prevalence of antibody to feline immunodeficiency virus in some cat populations. Veterinary Record 124, 397-398 Bergman, P.J., Camps-Palau, M.A., McKnight, J.A. et al. (2006) Development of a xenogeneic DNA vaccine program for canine malignant melanoma at the Animal Medical Centre. Vaccine 24, 4582-4585
- Bohm, M., Thompson, H., Weir, A. et al. (2004) Serum antibody titres to canine parvovirus, adenovirus and distemper virus in dogs in the UK which had not been vaccinated for at least three years. Veterinary Record 154, 457-463
- Bongiorno, G., Paparcone, R., Foglia Manzillo, V. et al. (2013) Vaccination with LiESP/QA-21 (CaniLeish®) reduces the intensity of infection in Phlebotomus perniciosusfed on Leishmania infantum infected dogs – a preliminary xenodiagnosis study. Veterinary Parasitology 197, 691-695
- Bragg, R. F., Duffy, A. L., DeCecco, F. A. et al. (2012) Clinical evaluation of a single dose of immune plasma for treatment of canine parvovirus infection. Journal of theAmerican Veterinary Medical Association 240, 700-704
- Brun, A., Chappuis G., Precausta, P. et al. (1979) Immunisation against panleukopenia: early development of immunity. Comparative Immunology, Microbiology and Infectious Diseases 1, 335-339
- Buonavoglia, C., Decaro, N., Martella, V. et al. (2006) Canine coronavirus highly pathogenic for dogs. Emerging Infectious Diseases 12 492-494
- Carpenter, J. W., Appel, M. J., Erickson, R. C. & Novilla, M. N. (1976) Fatal vaccine-induced canine distemper virus infection in black-footed ferrets. Journal of the American Veterinary Medical Association 169, 961-964
- Castleman, W. L., Powe, J. R., Crawford, P. C. et al. (2010) Canine H3N8 influenza virus infection in dogs and mice. Veterinary Pathology 47, 507-517
- Chang Fung Martel, J., Gummow, B., Burgess, G. et al. (2013) A door-to-door prevalence study of feline immunodeficiency virus in Australia. Journal of Feline Medicine and Surgery 15, 1070-1078
- Coleman, J. K., Pu, R., Martin, M. M. et al. (2014) Feline immunodeficiency virus (FIV) vaccine efficacy and FIV neutralizing antibodies. Vaccine 32, 746-754
- Connolly, M., Thomas, P., Woodroffe, R. & Raphael, B. L. (2013) Comparison of oral and intramuscular recombinant canine distemper vaccination in African wild dogs
- (Lycaon pictus). Journal of Zoo and Wildlife Medicine 44, 882-888
- Coyne, K. P., Dawson, S., Radford, A. D. et al. (2006a) Long-term analysis of feline calicivirus prevalence and viral shedding patterns in naturally infected colonies of domestic cats. Veterinary Microbiology 118, 12-25
- Coyne, K. P., Jones, B. R., Kipar, A. et al. (2006b) Lethal outbreak of disease associated with feline calicivirus infection in cats. Veterinary Record 158, 544-550 Crawford, P. C., Dubovi, E. J., Castleman, W. L. et al. (2005) Transmission of equine influenza virus to dogs. Science 310, 482-485
- Curtis, R. & Barnett, K. C. (1983) The ‘blue eye’ phenomenon. Veterinary Record 112, 347-353
- Daly, J. M., Blunden, A. S., Macrae, S. et al. (2008) Transmission of equine influenza virus to English foxhounds. Emerging Infectious Disease 14, 461-464
- Dawson, S., Willoughby, K., Gaskell, R. M. et al. (2001) A field trial to assess the effect of vaccination against feline herpesvirus, feline calicivirus and feline panleukopenia virus in 6-week-old kittens. Journal of Feline Medicine and Surgery 3, 17-22
- Day, M. J. (2010a) Ageing, immunosenescence and inflammageing in the dog and cat. Journal of Comparative Pathology 142 (Suppl. 1), S60-S69
- Day, M. J. (2010b) One health: the small companion animal dimension. Veterinary Record 167, 847-849
- Day, M. J., Breitschwerdt, E., Cleaveland, S. et al. (2012) Surveillance of zoonotic infectious diseases transmitted by small companion animals. Emerging Infectious Diseases. DOI:10.3201/eid1812.120664
- Day, M. J., Horzinek, M. & Schultz, R. D. (2007) Guidelines for the vaccination of dogs and cats. Journal of Small Animal Practice 48, 528-541
- Day, M. J., Horzinek, M. & Schultz, R. D. (2010) Guidelines for the vaccination of dogs and cats. Journal of Small Animal Practice 51, 338-356
- Day, M. J., Schoon, H.-A., Magnol, J.-P. et al. (2007) A kinetic study of histopathological changes in the subcutis of cats injected with non-adjuvanted and adjuvanted multi-component vaccines. Vaccine 25, 4073-4084
- Day, M. J. & Schultz, R. D. (2014) Vaccination. In: Veterinary Immunology: Principles and Practice, Taylor and Francis, Boca Raton, p. 224
- Dean, R. S., Pfeiffer, D. U. & Adams, V. J. (2013) The incidence of feline injection site sarcomas in the United Kingdom. BMC Veterinary Research 9, 17
- Decaro, N. & Buonavoglia, C. (2012) Canine parvovirus – a review of epidemiological and diagnostic aspects with emphasis on type 2c. Veterinary Microbiology 155,1-12
- Decaro, N., Crescenzo, G., Desario, C. et al. (2014) Long-term viraemia and fecal shedding in pups after modified-live canine parvovirus vaccination. Vaccine 32, 3850-3853
- Decaro, N., Desario, C. Elia, G. et al. (2008) Evidence for immunisation failure in vaccinated adult dogs infected with canine parvovirus type 2c. New Microbiology 31, 125-130
- Decaro, N., Mari, V., Campolo, M. et al. (2009) Recombinant canine coronaviruses related to transmissible gastroenteritis of swine are circulating in dogs. Journal of Virology 83, 1532-1537
- Deshpande, M. S., Jirjis, F. F., Tubbs, A. L. et al. (2009) Evaluation of the efficacy of a canine influenza virus (H3N8) vaccine in dogs following experimental challenge. Veterinary Therapeutics 10, 103-112
- DiGangi, B. A., Gray, L. K., Levy, J. K. et al. (2011) Detection of protective antibody titers against feline panleukopenia virus, feline herpesvirus-1, and feline calicivirus in shelter cats using a point-of-care ELISA. Journal of Feline Medicine and Surgery 13, 912-918
- DiGangi, B. A., Levy, J. K., Griffin, B. et al. (2012) Prevalence of serum antibody titers against feline panleukopenia virus, feline herpesvirus 1, and feline calicivirus in cats entering a Florida animal shelter. Journal of the American Veterinary Medical Association 241, 1320-1325
- Dodds, W. J. (2012) Immune plasma for treatment of parvoviral gastroenteritis. Journal of the American Veterinary Medical Association 240, 1056
- Dunham, S. P., Bruce, J., MacKay, S. et al. (2006) Limited efficacy of an inactivated feline immunodeficiency virus vaccine. Veterinary Record 158, 561-562 Durchfeld, B., Baumgartner, W., Herbst, W. & Brahm, R. (1990) Vaccine-associated canine distemper infection in a litter of African hunting dogs (Lycaon pictus). Zentralbl Veterinarmed B 37, 203-212
- Ellis, J. A. (2015) How well do vaccines for Bordetella bronchiseptica work in dogs? A critical review of the literature 1977-2014. Veterinary Journal 204, 5-16
- Ellis, J. A. & Krakowka, G. S. (2012) A review of canine parainfluenza virus infection in dogs. Journal of the American Veterinary Medical Association 240, 273-284
- Espinal, M. A., Diaz, F. J. & Ruiz-Saenz, J. (2014) Phylogenetic evidence of a new canine distemper virus lineage among domestic dogs in Colombia, South America. Veterinary Microbiology 172, 168-176
- Fernandes, C. B., Torres Magalhaes Jr, J., de Jesus, C. et al. (2104) Comparison of two commercial vaccines against visceral leishmaniasis in dogs from endemic areas: IgG, and subclasses, parasitism, and parasite transmission by xenodiagnosis. Vaccine 32, 1287-1295
- Fischer, S. M., Quest, C. M., Dubovi, E. J. et al. (2007) Response of feral cats to vaccination at the time of neutering. Journal of the American Veterinary Medical Association 230, 52-58
- Friedrich, K. & Truyen, U. (2000) Untersuchung der wirksamkeit von parvovirussimpfstoffen und der effektivitat zweier impfschemata. Praktischer Tierarzt 81, 988-994 Friend, S. C., Birch, C. J., Lording, P. M. et al. (1990) Feline immunodeficiency virus: prevalence, disease associations and isolation. Australian Veterinary Journal 67, 237-243
- Gaskell, R., Dawson, S., Radford, A. & Thiry, E. (2007) Feline herpesvirus. Veterinary Research 38, 337-354
- Gibbs, E. P. J. (2014) The evolution of One Health: a decade of progress and challenges for the future. Veterinary Record 174, 85-91
- Gleich, S. E., Krieger, S. & Hartmann, K. (2009) Prevalence of feline immunodeficiency virus and feline leukaemia virus among client-owned cats and risk factors for infection in Germany. Journal of Feline Medicine and Surgery 11, 985-992
- Glennon, P. J., Cockburn, T. & Stark, D. M. (1991) Prevalence of feline immunodeficiency virus and feline leukemia virus infections in random-source cats. Laboratory Animal Science 41, 545-547
- Gobar, G. M. & Kass, P. H. (2002) World Wide Web-based survey of vaccination practices, postvaccinal reactions, and vaccine site-associated sarcomas in cats. Journal of the American Veterinary Medical Association 220, 1477-1482
- Gordon, J. C. & Angrick, E. J. (1986) Canine parvovirus: environmental effects on infectivity. American Journal of Veterinary Research 47, 1464-1467
- Gray, L. K., Crawford, P. C., Levy, J. K. et al. (2012) Comparison of two assays for detection of antibodies against canine parvovirus and canine distemper virus in dogs admitted to a Florida animal shelter. Journal of the American Veterinary Medical Association 240, 1084-1087
- Grosenbaugh, D. A., Leard, A. T., Bergman, P. J. et al. (2011) Safety and efficacy of a xenogeneic DNA vaccine encoding for human tyrosinase as adjunctive treatment for oral malignant melanoma in dogs following surgical excision of the primary tumor. American Journal of Veterinary Research 72, 1631-1638
- Hartman, E. G., van Houten, M., Frik, J. F. & van der Donk, J. A. (1984) Humoral immune response of dogs after vaccination against leptospirosis measured by an IgM- and IgG-specific ELISA. Veterinary Immunology and Immunopathology 7, 245-254
- Hartmann, K., Day, M. J., Thiry, E., et al. (2015) Feline injection site sarcoma: ABCD guidelines on prevention and management. Journal of Feline Medicine and Surgery 17, 606-613.
- Hendricks, C. G., Levy, J. K., Tucker, S. J. et al. (2014) Tail vaccination in cats: a pilot study. Journal of Feline Medicine and Surgery 16, 275-280
- Hess, T. J., Parker, D. S., Hassall, A. J. & Chiang, Y. W. (2011) Evaluation of efficacy of oral administration of Bordetella intranasal vaccine when used to protect puppies from tracheobronchitis due to B. Bronchiseptica infection. International Journal of Applied Research in Veterinary Medicine 9, 301-305
- Hitt, M. E., Spangler, L. & McCarville, C. (1992) Prevalence of feline immunodeficiency virus in submissions of feline serum to a diagnostic laboratory in Atlantic Canada. Canadian Veterinary Journal 33, 723-726
- Hoare, C. M., DeBouck, P. & Wiseman, A. (1997) Immuonogenicity of a low-passage, high-titer modified live canine parvovirus vaccine in pups with maternally derived antibodies. Vaccine 15, 273-275
- Hofmann-Lehmann, R., Fehr, D., Grob, M. et al. (1996) Prevalence of antibodies to feline parvovirus, calicivirus, herpesvirus, coronavirus, and immunodeficiency virus and of feline leukemia virus antigen and the interrelationship of these viral infections in free-ranging lions in east Africa. Clinical and Diagnostic Laboratory Immunology 3, 554-562
- Horzinek, M. C. (2010) Vaccination protocols for companion animals: the veterinarian’s perspective. Journal of Comparative Pathology 142 (Suppl. 1), S129-S132 Hosie, M. J., Addie, D., Belak, S. et al. (2013) Matrix vaccination guidelines: ABCD recommendations for indoor/outdoor cats, rescue shelter cats and breeding catteries. Journal of Feline Medicine and Surgery 15, 540-544
- Hosie, M. J. & Beatty, J. A. (2007) Vaccine protection against feline immunodeficiency virus: setting the challenge. Australian Veterinary Journal 85, 5-12
- Hosie, M. J., Osborne, R., Yamamoto, J. K. et al. (1995) Protection against homologous but not heterologous challenge induced by inactivated feline immunodeficiency virus vaccines. Journal of Virology 69, 1253-1255
- Hosie, M. J., Robertson, C. & Jarrett, O. (1989) Prevalence of feline leukaemia virus and antibodies to feline immunodeficiency virus in cats in the United Kingdom.Veterinary Record 125, 293-297
- Houston, D. M., Ribble, C. S. & Head, L. L. (1996) Risk factors associated with parvovirus enteritis in dogs: 283 cases (1982-1991). Journal of the American Veterinary Medical Association 208, 542-546
- Huang, C., Hess, J., Gill, M. et al. (2010) A dual-strain feline calicivirus vaccine stimulates broader cross-neutralization antibodies than a single-strain vaccine and lessens clinical signs in vaccinated cats when challenged with a homologous feline calicivirus strain associated with virulent systemic disease. Journal of Feline Medicine and Surgery 12, 129-137
- Jakel, V., Cussler, K., Hanschmann, K. M. et al. (2012) Vaccination against feline panleukopenia: implications from a field study in kittens. BMC Veterinary Research 8, 62
- Jas, D., Coupier, C., Edlund Toulemonde, E. et al. (2012) Three-year duration of immunity in cats vaccinated with a canarypox-vectored recombinant rabies virus vaccine. Vaccine 30, 6991-6996
- Jas, D., Frances-Duvert, V., Vernes, D. et al. (2015) Three-year duration of immunity for feline herpesvirus and calicivirus evaluated in a controlled vaccination-challenge laboratory trial. Veterinary Microbiology 177, 123-131
- Johnson, R. P. & Povey, R. C. (1983) Transfer and decline of maternal antibody to feline calicivirus. Canadian Veterinary Journal 24, 6-9
- Jones, B. R., Hodge, H. & Davies, E. (1995) The prevalence of feline immunodeficiency virus infection in hyperthyroid cats. New Zealand Veterinary Journal 43, 23-24 Kapil, S., Allison, R. W., Johnston III, L. et al. (2008) Canine distemper virus strains circulating among North American dogs. Clinical and Vaccine Immunology 15,707-712
- Kass, P. H., Barnes, W. G., Jr., Spangler, W. L. et al. (1993) Epidemiologic evidence for a causal relation between vaccination and fibrosarcoma tumorigenesis in cats. Journal of the American Veterinary Medical Association 203, 396-405
- Kennedy, L. J., Lunt, M., Barnes, A. et al. (2007) Factors influencing the antibody response of dogs vaccinated against rabies. Vaccine 25, 8500-8507
- Kirkland, P. D., Finlaison, D. S., Crispe, E. & Hurt, A. C. (2010) Influenza virus transmission from horses to dogs, Australia. Emerging Infectious Diseases 16, 699-702 Klaasen, H. L., Molkenboer, M. J., Vrijenhoek, M. P. & Kaashoek, M. J. (2003) Duration of immunity in dogs vaccinated against leptospirosis with a bivalent inactivatedvaccine. Veterinary Microbiology 95, 121-132
- Klassen, H. L. B. M., van der Veen, M., Molkenboer M. J. C. H. et al. (2012) A novel tetravalent Leptospira bacterin protects against infection and shedding following challenge in dogs. Veterinary Record 172, 181
- Klaasen, H. L. B. M., van der Veen, M., Sutton, D. et al. (2014) A new tetravalent canine leptospirosis vaccine provides at least 12 months immunity against infection.Veterinary Immunology and Immunopathology 158, 26-29
- Korbelik, J., Rand, J. S. & Morton, J. M. (2011) Comparison of early socialization practices used for litters of small-scale registered dog breeders and nonregistered dogs breeders. Journal of the American Veterinary Medical Association 239, 1090-1097
- Kusuhara, H., Hohdatsu, T., Seta, T. et al. (2007) Serological differentiation of FIV-infected cats from dual-subtype feline immunodeficiency virus vaccine (Fel-O-Vax FIV) inoculated cats. Veterinary Microbiology 120, 217-225
- Ladlow, J. (2013) Injection site-associated sarcoma in the cat: treatment recommendations and results to date. Journal of Feline Medicine and Surgery 15, 409-418
- Lappin, M. R. (2012) Feline panleukopenia virus, feline herpesvirus-1 and feline calicivirus antibody responses in seronegative specific pathogen-free kittens after parenteral administration of an inactivated FVRCP vaccine or a modified live FVRCP vaccine. Journal of Feline Medicine and Surgery 14, 161-164
- Lappin, M. R., Andrews, J., Simpson, D. & Jensen, W. A. (2002) Use of serologic tests to predict resistance to feline herpesvirus 1, feline calicivirus, and feline parvovirus infection in cats. Journal of the American Veterinary Medical Association 220, 38-42
- Lappin, M. R., Sebring, R. W., Porter, M. et al. (2006) Effects of a single dose of an intranasal feline herpesvirus 1, calicivirus, and panleukopenia vaccine on clinical signs and virus shedding after challenge with virulent feline herpesvirus 1. Journal of Feline Medicine and Surgery 8, 158-163
- Lappin, M. R., Veir, J. Hawley, J. (2009) Feline panleukopenia virus, feline herpesvirus-1, and feline calicivirus antibody responses in seronegative specific pathogen-free cats after a single administration of two different modified live FVRCP vaccines. Journal of Feline Medicine and Surgery 11, 159-162
- Larson, L. J., Henningson, J., Sharp, P. et al. (2011) Efficacy of the canine influenza virus H3N8 vaccine to decrease severity of clinical disease after co-challenge with canine influenza virus and Streptococcus equi subsp. zooepidemicus. Clinical and Vaccine Immunology 18, 559-564
- Larson, L. J. & Schultz, R. D. (2006) Effect of vaccination with recombinant canine distemper virus vaccine immediately before exposure under shelter-like conditions. Veterinary Therapeutics 7, 113-118
- Larson, L. J., Henningson, J., Sharp, P. et al. (2011) Efficacy of the canine influenza virus H3N8 vaccine to decrease severity of clinical disease after co-challenge with canine influenza virus and Streptococcus equi subsp. zooepidemicus. Clinical and Vaccine Immunology 18, 559-564
- Larson, L. J. & Schultz, R. D. (2006) Effect of vaccination with recombinant canine distemper virus vaccine immediately before exposure under shelter-like conditions.Veterinary Therapeutics 7, 113-118
- Lee, I. T., Levy, J. K., Gorman, S. P. et al. (2002) Prevalence of feline leukemia virus infection and serum antibodies against feline immunodeficiency virus in unownedfree-roaming cats. Journal of the American Veterinary Medical Association 220, 620-622
- Lechner, E. S., Crawford, P. C., Levy, J. K. et al. (2010) Prevalence of protective antibody titers for canine distemper virus and canine parvovirus in dogs entering a Florida animal shelter. Journal of the American Veterinary Medical Association 236, 1317-1321
- Levy, J. K., Crawford, P. C., Kusuhara, H. et al. (2008) Differentiation of feline immunodeficiency virus vaccination, infection, or vaccination and infection in cats. Journalof Veterinary Internal Medicine 22, 330-334
- Litster, A., Nichols, J. & Volpe, A. (2012) Prevalence of positive antibody test results for canine parvovirus (CPV) and canine distemper virus (CDV) and response to modified live vaccination against CPV and CDV in dogs entering animal shelters. Veterinary Microbiology 157, 86-90
- Lloret, A. (2009) The process of evidence-based medicine. Journal of Feline Medicine and Surgery 11, 529
- Maes, R. (2012) Felid herpesvirus type 1 infection in cats: a natural host model for alphaherpesvirus pathogenesis. ISRN Veterinary Science 2012, 495830 Martano, M., Morello, E. & Buracco, P. (2011) Feline injection-site sarcoma: past, present and future perspectives. Veterinary Journal 188, 136-141
- Martin, L. E. R., Wiggans, K. T., Wennogle, S. A. et al. (2014) Vaccine-associated Leptospira antibodies in client-owned dogs. Journal of Veterinary Internal Medicine 28, 789-792
- Meichner, K., Kruse, D. B., Hirschberger, J. & Hartmann, K. (2012) Changes in prevalence of progressive feline leukaemia virus infection in cats with lymphoma inGermany. Veterinary Record 171, 348
- Mende, K., Stuetzer, B., Truyen, U. et al. (2014) Evaluation of an in-house dot enzyme-linked immunosorbent assay to detect antibodies against feline panleukopenia virus. Journal of Feline Medicine and Surgery, in press
- Mitchell, S. A., Zwijnenberg, R. J., Huang, J. et al. (2012) Duration of serological response to canine parvovirus-type 2, canine distemper virus, canine adenovirus-type 1 and canine parainfluenza virus in client-owned dogs in Australia. Australian Veterinary Journal 90, 468-473
- Miyaji, K., Suzuki, A., Shimakura, H. et al. (2012) Large-scale survey of adverse reactions to canine non-rabies combined vaccines in Japan. Veterinary Immunology and Immunopathology 145, 447-452
- Moore, G. E., Guptill, L. F., Ward, M. P. et al. (2005) Adverse events diagnosed within three days of vaccine administration in dogs. Journal of the American Veterinary Medical Association 227, 1102-1108
- Moore, G. E., DeSantis-Kerr, A. C., Guptill, L. F. et al. (2007) Adverse events after vaccine administration in cats: 2560 cases (2002-2005). Journal of the American Veterinary Medical Association 231, 94-100
- Moreno, J., Vouldoukis, I., Schreiber, P. et al. (2014) Primary vaccination with the LiESP/QA-21 vaccine (CaniLeish®) produces a cell-mediated immune response which is still present 1 year later. Veterinary Immunology and Immunopathology 158, 199-207
- Morton, J. M., McCoy, R. J., Kann, R. K. et al. (2012) Validation of real-time polymerase chain reaction tests for diagnosing feline immunodeficiency virus infection in cats using Bayesian latent class models. Preventive Veterinary Medicine 104, 136-148
- Mouzin, D. E., Lorenzen, M. J., Haworth, J. D. & King, V. L. (2004) Duration of serologic response to five viral antigens in dogs. Journal of the American Veterinary Medical Association 224, 55-60
- Muirden, A. (2002) Prevalence of feline leukaemia virus and antibodies to feline immunodeficiency virus and feline coronavirus in stray cats sent to an RSPCA hospital. Veterinary Record 150, 621-625
- Norris, J. M., Bell, E. T., Hales, L. et al. (2007) Prevalence of feline immunodeficiency virus infection in domesticated and feral cats in eastern Australia. Journal of Feline Medicine and Surgery 9, 300-308
- Ohneiser, S. A., Hills, S. F., Cave, N. J. et al. (2015) Canine parvoviruses in New Zealand form a monophyletic group distinct from the viruses circulating in other parts of the world. Veterinary Microbiology (in press).
- Ottnod, J. M., Smedley, R. C., Walshaw, R. et al. (2013) A retrospective analysis of the efficacy of Oncept vaccine for the adjunct treatment of canine oral malignant melanoma. Veterinary and Comparative Oncology 11, 219-229
- Palatnik-de-Sousa, C.B. & Day, M. J. (2011) One health: the global challenge of epidemic and endemic leishmaniasis. Parasites and Vectors 4,197
- Palatnik-de-Sousa, C.B., Silva-Antunes, I., de Aguiar Morgado, A. et al. (2009) Decrease of the incidence of human and canine visceral leishmaniasis after dog vaccination with Leishmune® in Brazilian endemic areas. Vaccine 27, 3505-3512
- Payungporn, S., Crawford, P. C., Kouo, T. S. et al. (2008) Influenza A virus (H3N8) in dogs with respiratory disease, Florida. Emerging Infectious Diseases 14, 902-908 Pearson, G. L. (1977) Vaccine-induced canine distemper virus in black-footed ferrets. Journal of the American Veterinary Medical Association 170, 103-109 Pedersen, N. C., Elliott, J. B., Glasgow, A. et al. (2000) An isolated epizootic of hemorrhagic-like fever in cats caused by a novel and highly virulent strain of feline
- calicivirus. Veterinary Microbiology 73, 281-300
- Pollock, R. V. & Carmichael, L. E. (1982a) Maternally derived immunity to canine parvovirus infection: transfer, decline, and interference with vaccination. Journal of the American Veterinary Medical Association 180, 37-42
- Pollock, R. V. & Carmichael, L. E. (1982b) Dog response to inactivated canine parvovirus and feline panleukopenia virus vaccines. Cornell Veterinarian 72, 16-35 Poulet, H., Brunet, S., Leroy, V. et al. (2005) Immunisation with a combination of two complementary feline calicivirus strains induces a broad cross-protection against heterologous challenges. Veterinary Microbiology 106, 17-31
- Poulet, H., Jas, D., Lemeter, C. et al. (2008) Efficacy of a bivalent inactivated non-adjuvanted feline calicivirus vaccine: relation between in vitro cross-neutralization and heterologous protection in vivo. Vaccine 26, 3647-3654
- Pratelli, A. & Colao, V. (2014) A population prevalence study on influenza infection in dogs in Southern Italy. New Microbiologica 37, 277-283
- Ravi, M., Wobeser, G. A., Taylor, S. M. & Jackson, M. L. (2010) Naturally acquired feline immunodeficiency virus (FIV) infection in cats from western Canada: prevalence,
- disease associations, and survival analysis. Canadian Veterinary Journal 51, 271-276
- Reagan, K. L., Hawley, J. R. & Lappin, M. R. (2014) Concurrent administration of an intranasal vaccine containing feline herpesvirus-1 (FHV-1) with a parenteral vaccine containing FHV-1 is superior to parenteral vaccination alone in an acute FHV-1 challenge model. Veterinary Journal 201, 202-206
- Richter, M., Schudel, L., Tobler, K. et al. (2009) Clinical, virological, and immunological parameters associated with superinfection of latently with FeHV-1 infected cats.Veterinary Microbiology 138, 205-216
- Roberts, E. S., VanLare, K. A., Roycroft, L. M. & King, S. (2015) Effect of high-dose ciclosporin on the immune response to primary and booster vaccination in immunocompetent cats. Journal of Feline Medicine and Surgery 17, 101-109
- Rypula, K., Ploneczka-Janeczko, K., Bierowiec, K. et al. (2014) Prevalence of viral infections in cats in southwestern Poland in the years 2006 to 2010. Berl Munch Tierarztl Wochenschr 127, 163-165
- Sachse, K., Bavoil, P. M., Kaltenboeck, B. et al. (2015) Emendation of the family Chlamydiaceae: proposal of a single genus, Chlamydia to include all currently recognized species. Systemic and Applied Microbiology 38, 99-103
- Schorr-Evans, E. M., Poland, A., Johnson, W. E. & Pedersen, N. C. (2003) An epizootic of highly virulent feline calicivirus disease in a hospital setting in New England.
- Schulz, B., Klinkenberg, C., Fux, R. et al. (2014) Prevalence of canine influenza virus A (H3N8) in dogs in Germany. Veterinary Journal 202, 184-185
- Schultz, R. D. (2006) Duration of immunity for canine and feline vaccines: a review. Veterinary Microbiology 117, 75-79
- Schultz, R. D. (2009) A commentary on parvovirus vaccination. Journal of Feline Medicine and Surgery 11, 163-164
- Schultz, R. D. & Larson, L. J. (1996) The new generation of parvovirus vaccines. A comparison study. Compendium of Continuing Education for the Practicing Veterinarian 18, 640-641
- Schultz, R. D., Thiel, B., Mukhtar, E. et al. (2010) Age and long-term protective immunity in dogs and cats. Journal of Comparative Pathology 142 (Suppl. 1), S102-S108 Scott, F. W. & Geissinger, C. M. (1997) Duration of immunity in cats vaccinated with an inactivated feline panleukopenia, herpesvirus and calicivirus vaccine. Feline Practice 25, 12-19
- Scott, F. W. & Geissinger, C. M. (1999) Long-term immunity in cats vaccinated with an inactivated trivalent vaccine. American Journal of Veterinary Research 60, 652-658
- Scherk, M. A., Ford, R. B., Gaskell, R. M. et al. (2013) 2013 AAFP Feline Vaccination Advisory Panel report. Journal of Feline Medicine and Surgery 15, 785-808 Schuller, S., Francey, T., Hartmann, K. et al. (2015) European consensus statement on leptospirosis in dogs and cats. Journal of Small Animal Practice 56, 159-179 Shaw, S. C., Kent, M. S., Gordon, I. K. et al. (2009) Temporal changes in characteristics of injection-site sarcomas in cats: 392 cases (1990-2006). Journal of the
- American Veterinary Medical Association 234, 376-380
- Spibey, N., Greenwood, N. M., Sutton, D. et al. (2008) Canine parvovirus type 2 vaccine protects against virulent challenge with type 2c virus. Veterinary Microbiology 128, 48-55
- Srivastav, A., Kass, P. H., McGill, L. D. et al. (2012) Comparative vaccine-specific and other injectable-specific risks of injection-site sarcomas in cats. Journal of the American Veterinary Medical Association 241, 595-602
- Stepita, M. E., Bain, M. J. & Kass, P. H. (2013) Frequency of CPV infection in vaccinated puppies that attended puppy socialization classes. Journal of the American Animal Hospital Association 49, 95-100
- Strasser, A., May, B., Teltscher, A. et al. (2003) Immune modulation following immunization with polyvalent vaccines in dogs. Veterinar y Immunology and Immunopathology 94, 113-121
- Thiry, E. & Horzinek, M. C. (2007) Vaccination guidelines: a bridge between official requirements and the daily use of vaccines. Revue Scientifique et Technique de l’Office International des Épizooties 26, 511-517
- Ueland, K. & Lutz, H. (1992) Prevalence of feline leukemia virus and antibodies to feline immunodeficiency virus in cats in Norway. Zentralblatt für Veterinärmedizin.
- Reihe B. Journal of Veterinary Medicine. Series B 39, 53-58
- Wang, C., Johnson, C. M., Ahluwalia, S. K. et al. (2010) Dual-emission fluorescence resonance energy transfer (FRET) real-time PCR differentiates feline immunodeficiency virus subtypes and discriminates infected from vaccinated cats. Journal of Clinical Microbiology 48, 1667-1672
- Weijer, K. & Daams, J. H. (1976) The presence of leukaemia (lymphosarcoma) and feline leukaemia virus (FeLV) in cats in The Netherlands. Journal of Small Animal Practice 17, 649-659
- Weijer, K., UijtdeHaag, F. & Osterhaus, A. (1986) Control of feline leukaemia virus infection by a removal programme. Veterinary Record 119, 555-556
- Weijer, K., Uytdehaag, F. G. & Osterhaus, A. D. (1989) Control of feline leukaemia virus. Veterinary Immunology and Immunopathology 21, 69-83
- Welborn, L. V., DeVries, J. G., Ford, R. et al. (2011) 2011 AAHA canine vaccination guidelines. Journal of the American Animal Hospital Association 47, 1-42 Westman, M. E., Malik, R., Hall, E. et al. (2015) Determining the feline immunodeficiency virus (FIV) status of FIV-vaccinated cats using point-of-care antibody kits.
- Comparative Immunology, Microbiology and Infectious Diseases.
- Wilson, S., Stirling, C., Borowski S. et al. (2013) Vaccination of dogs with Duramune DAPPi+LC protects against pathogenic canine parvovirus type 2c challenge.Veterinary Record 172, 662
- Wilson, S., Stirling, C., Thomas, A. et al. (2013) Duration of immunity of a multivalent (DHPPi/L4R) canine vaccine against four Leptospira serovars. Vaccine 31, 3126-3130
- Yamamoto, J. K., Pu, R., Sato, E. & Hohdatsu, T. (2007) Feline immunodeficiency virus pathogenesis and development of a dual-subtype feline-immunodeficiency-virus vaccine. AIDS 21, 547-563
- Yilmaz, H., Ilgaz, A. & Harbour, D. A. (2000) Prevalence of FIV and FeLV infections in cats in Istanbul. Journal of Feline Medicine and Surgery 2, 69-70